Проблема побочного действия лекарственных веществ привлекает все большее внимание, приобретая медико-социальное значение в связи с нарастающим потоком поступления новых медикаментов и увеличением числа осложнений. Различные причины ведут к побочным реакциям при использовании медикаментов, и особенности фармакологического действия самого лекарственного препарата в терапевтических дозах не всегда определяют их. Назначение нескольких лекарственных препаратов одновременно при плохом представлении об их взаимодействии между собой, препаратов иногда не самого лучшего качества усугубляется наступательной рекламной политикой фармацевтических компаний. Поток рекламной информации в публикациях, по телевидению и в Интернет усиливается выступлениями некоторых врачей, в корыстных целях на симпозиумах и конференциях превозносящих достоинства того или иного препарата. Нередко фармацевтические фирмы спонсируют научные исследования, а «кто платит, тот и заказываем музыку». Не случайно в последние 2-3 года в зарубежной литературе появились статьи, в которых проводится мысль, что клиника при СПИДе определяется не самим вирусом, а теми побочными эффектами, которыми обладают весьма токсичные антиретровирусные препараты. По мнению авторов, фармацевтические фирмы потратили миллионы на разработку химиопрепаратов – ингибиторов обратной транскриптазы и протеазы ВИЧ и ученые-разработчики «отрабатывают» затраты через средства массовой информации, профессиональные журналы, съезды и симпозиумы создавая этим препаратам рекламу. Мы далеки от подобных обвинений в отношении антиретровирусных препаратов, но сама идея возможности подобного в медицинской науке не так уж далека от истины. В нашей стране с учетом того факта, что государственное финансирование науки почти прекратилось, почва для подобной ситуации имеется.
Наконец, необходимо учитывать и тот факт, что при назначении лекарственных средств врач ориентируется только на инструкцию, представленную фармацевтической фирмой, а последняя не всегда объективно отражает информацию о побочных действиях.
Несмотря на предпринимаемые шаги по контролю за побочными эффектами лекарственной терапии во многих странах, состояние регистрации побочного действия лекарств и медикаментозных осложнений не дает возможности правильно оценить проблему. Проведенные в США исследования показали, что целенаправленное выявление побочных реакций в 85 хирургических и 67 терапевтических больницах в течение 21 дня выявило побочные реакции в 7,1 % случаев. в то время как добровольная система сообщений врачами и медицинскими сестрами за 45-дневный период наблюдений выявила медикаментозные реакции лишь в 0,08 %, что в 88,7 раз меньше. Поэтому Leape L.L. et al. (1995), Lazarou J. et al. (1998), Cohen J.S. (1999) и многие другие специалисты по изучению побочных реакций на лекарственные средства полагают, что система выявления не только медикаментозных осложнений, но и всех побочных реакций должна носить унифицированный характер.
О том же положении свидетельствуют данные Подкомитета по нежелательным лекарственным реакциям при Комитете по безопасности лекарств Великобритании. При 1,5 млн. выписанных за год рецептов на дегидрокодеин поступило лишь 32 сообщения о побочных реакциях, в то же время даже у практически здоровых людей этот препарат вызывает побочные реакции в 10 % случаев. Следовательно, побочных реакций зарегистрировано почти в 5 тыс. раз меньше, чем можно было ожидать.
Отсутствие четкой регистрации медикаментозных осложнений во многом объясняется трудностями дифференциации их от клинических проявлений заболевания, по поводу которого назначаются лекарственные препараты. Если токсико-аллергические проявления действия медикаментозных препаратов с локализацией на коже и слизистых оболочках сравнительно легко диагностируются, то токсические реакции со стороны паренхиматозных органов, общеорганизменные проявления трудно отличить от самостоятельных заболеваний этих органов. Некоторые осложнения проявляются через годы после приема лекарств.
При проведении медикаментозной терапии всегда присутствует риск нежелательных эффектов. Согласно статистике, в среднем побочные реакции возникают у 10-20 % госпитализированных больных, в развивающихся странах этот показатель составляет 30-40%. Так, по данным K.L. Melmon (1998), у 18 - 30 % больных возникают различные побочные реакции на лекарства, а 3-5% больных госпитализируются именно из-за развившихся осложнений. Наибольший процент составляют аллергические реакции. В США вследствие развития побочных реакций ежегодно госпитализируется от 3,5 до 8,8 млн. человек, от лекарственных осложнений ежегодно умирает до 200 тысяч человек. В Молдове Информационный фармакологический Центр "DRUGS" представил результаты собственного исследования, проводимого в 1995-96 гг. среди врачей республики. По результатам анкетирования 605 врачей различных регионов республики 39% из них не знают кому сообщать о выявленных побочных реакциях на лекарства; остальные врачи делятся подобной информацией в основном с коллегами по работе (60 %), а также сообщают администрации (42 %) и лишь 7 % из них предоставляют сведения больничным фармацевтам. На сегодняшний день нет взаимного обмена информацией между врачом и фармацевтом.
В клинической практике весьма трудно четко определить, являются ли имеющиеся симптомы проявлением основного заболевания, по поводу которого назначена терапия или они возникли в результате медикаментозного осложнения. В связи с необходимостью комплексной терапии больных большие трудности представляет также вопрос выявления из нескольких лекарств препарата, послужившего причиной побочной реакции и осложнения. Так, изучив 1932 случая смерти (с различной степенью доказанности роли медикаментозных осложнений) за 10 лет в США, N. Irey (1976) установил, что 43 % составили доказанные и возможные патологические реакции, 35 % — вероятные, 16 % — случайные, остальные — отрицательные. Из доказанных и возможных патологических лекарственных реакций чаще всего причиной смерти была передозировка, случайная или с суицидальной целью (табл.25).
Обычно абсолютная передозировка встречается редко, в основном как следствие ошибки медицинских и аптечных работников или суицидального умысла самого больного. Относительная передозировка возникает при использовании среднетерапевтических доз у больных с заболеваниями определенных органов и систем, ответственных за обезвреживание или выделение лекарственных препаратов, прежде всего, почек и печени.
Таблица 25
Разграничения побочных реакций (по N. Irey, 1976)
|
Группа |
Кол-во случаев, абсолютные числа |
% |
|
Передозировка случайная или с суицидальной целью
|
428
|
51,8
|
|
Осложнения, вызванные противоопухолевыми цитостатиками
|
48
|
5,7
|
|
Побочные реакции на бытовые химикаты
|
19
|
2,3
|
|
Медикаментозные реакции легкой и средней степени
|
65
|
7,9
|
|
Тяжелые и летальные медикаментозные реакции, возникшие при терапии тяжелого или неизлечимого основного заболевания
|
22
|
2,6
|
|
Летальные медикаментозные реакции, связанные с диагностическими или терапевтическими мерами
|
25
|
3,0
|
|
Побочные медикаментозные реакции как неожиданно вредные, проявляющиеся при назначении терапевтических доз препаратов с целью профилактики, диагностики или лечения
|
220
|
26,6
|
В группе летальных медикаментозных реакций, связанных с диагностическими или терапевтическими мерами, по данным N. Irey, основными причинами осложнений были: а) игнорирование опасных симптомов в анамнезе или результатов лабораторных анализов; б) отсутствие преемственности в лечении больных; в) применение потенциально опасных препаратов с необоснованным риском; г) невыявленная возможность взаимовлияний комплекса лекарств; д) назначение лекарств, обладающих кумуляцией или вызывающих привыкание; е) технические погрешности, связанные с маркировкой лекарств; ж) самолечение; з) игнорирование указаний к запрещению длительного применения лекарств, свободно продающихся без рецептов.
Среди побочных медикаментозных реакций, как неожиданно вредных, чаще всего встречались медикаментозные поражения печени, костного мозга, сердечно-сосудистой системы, почек, центральной нервной системы, желудочно-кишечного тракта. Из всех побочных реакций 30 % были тяжелыми, почти 70% — средней тяжести.
По данным Шведского комитета нежелательных лекарственных реакций, за 5 лет исследования поступило 4362 сообщения о побочных реакциях и осложнениях. Среди осложнений чаще всего регистрировались поражения кожи (25 %), печени (13), тромбоэмболические (10) и гематологические (10) осложнения. Среди лекарственных препаратов, обусловивших осложнения, чаще всего регистрировались оральные контрацептивы (25), химио-терапевтические препараты (19), анальгетики (14), психотропные средства (12) и препараты, действующие на сердечно-сосудистую систему (9 %). В 3,2 % случаев медикаментозные осложнения закончились летально, причем в 48% летальный исход был обусловлен гематологическими осложнениями, в 13 – в результате тромбоэмболии, в 9 – от анафилактического шока и в 7 % смерть наступила от печеночных осложнений. Чаще всего ее причиной служили антибиотики, противовоспалительные препараты, оральные контрацептивы, психотропные лекарственные вещества и сульфаниламиды.
В Англии, по сообщению W. Inman (1973), из 626 случаев побочных реакций на медикаменты больше всего (200) осложнений развилось при применении трициклических антидепрессантов. Фенилбутазон (бутадион) и оксифенилбутазон явились причиной тяжелых поражений крови у 36 % больных, в большинстве со смертельными исходами. Эти же препараты в 20 % случаев вызвали осложнения со стороны желудочно-кишечного тракта и в одной трети случаев закончились летально. Довольно часто гематологические (8 %) и желудочно-кишечные (17 %) осложнения вызывал индометацин, причем почти у четверти больных при гематологических и у 40% при желудочно-кишечных осложнениях исход был летальным.
По данным отчета Австралийского консультативного комитета по побочным лекарственным реакциям за год получено по стране 1870 сообщений о побочных реакциях. Больше всего из них зарегистрировано реакций на сульфаметоксазол (123 сообщения) и ампициллин (106). Из клинических проявлений чаще отмечались сыпь (498), зуд (173), крапивница (163), тошнота (146), артериальная гипотония (45), бронхоспазм (40), тахикардия (28), пурпура (23), анафилактический шок (21), тромбоцитопения (20), артериальная гипертония (17), артралгия (15), многоформная эритема (15), нейтропения (15), анемия (14), агранулоцитоз (12), лейкопения (11), псевдомембранозный колит. Соотношение мужчины/женщины составляло 1:1,5. Из общего числа осложнений 11 смертельных исходов.
Довольно часто медикаментозные осложнения встречаются в пожилом возрасте. По вполне понятным причинам люди в этом возрасте более часто и в большем количестве потребляют лекарственные вещества, получают медикаментозное лечение. В США люди пожилого возраста составляют 10% населения, потребляя при этом 25 % всех выписываемых медикаментов [Fischer L.R. et al., 2000]. Именно среди этого контингента людей чаще всего распространено злоупотребление лекарственными препаратами, самолечение, прием препаратов в течение длительных сроков, необоснованная приверженность к некоторым препаратам и одновременное употребление нескольких медикаментов. Исследования показали, что при одномоментном приеме 4—5 медикаментов в 4,2 % случаев обнаруживаются реакции взаимодействия, в то-время, как при приеме 20 препаратов их частота возрастает до 45 %.
В связи с тем, что примерно 40 % пожилых людей применяют нейролептики и антидепрессанты, еще больше – ацетилсалициловую кислоту у них часто отмечается ослабление перистальтики желудка и кишечника, благоприятствующее более полному всасыванию принятых лекарств и создающее угрозу увеличения токсического эффекта. В крови у пожилых людей содержание белков плазмы снижено. Это способствует накоплению в ней повышенных концентраций лекарственных веществ, не связанных с белком, что также увеличивает опасность токсического эффекта.
Многие барбитураты, а также некоторые другие лекарственные вещества, широко применяемые пожилыми людьми, являются ферментативными индукторами, активизируют метаболические процессы и в силу этого ускоряют инактивацию одновременно с ними принятых лекарственных веществ. Возникает потребность увеличения дозы препаратов. Если же фенобарбитал или другой препарат-индуктор отменяются, но продолжается введение остальных медикаментов, может наступить токсическое осложнение. Так, частое сочетанное применение барбитуратов с антикоагулянтами в случае отмены барбитуратов приводит к геморрагическим осложнениям.
Наконец, у пожилых людей в силу уменьшения почечного кровотока, клубочковой фильтрации и канальцевой секреции создаются условия для кумуляции, опасные при сочетанном применении нескольких препаратов.
Лекарства различных групп не одинаково часто приводят к побочным реакциям и медикаментозным осложнениям, что связано не только с фармакологическим эффектом самого препарата, но и с интенсивностью его употребления в клинической практике. По статистическим данным, чаще всего в стационаре приходится встречаться с осложнениями, вызванными противомикробными и противопаразитарными препаратами.
Рост побочных реакций при терапии антимикробными средствами связан с нерациональным использованием их, зачастую с применением максимальных доз, неоправданное увеличение курса лечения и кратности применения препаратов. Побочные эффекты, обусловленные антимикробными препаратами В.Ф. Ковалев и соавт. (1988) подразделяют на три группы в зависимости от механизма действия препарата на макроорганизм:
1. Реакции за счет повышенной индивидуальной или видо-возрастной чувствительности животных к противомикробным препаратам (аллергические реакции), вызванные идиосинкразией или сенсибилизацией организма к лекарственному соединению. Этот тип реакций обычно не связан с количеством введенного препарата, а тяжесть поражений широко варьирует от легких кожных реакций до анафилактического шока с летальным исходом.
2. Прямые токсические реакции, связанные с количеством введенного препарата и обусловленные органотропностью и специфичностью действия лекарственного вещества на макроорганизм. Наиболее часто при этом типе реакций поражаются почки, печень, нервная и кроветворная системы, а также желудочно-кишечный тракт.
3. Реакции за счет биологических изменений в микроорганизме или в микробном агенте. К этому типу реакций относят: образование лекарственно-устойчивых штаммов возбудителей, суперинфекцию, дисбактериоз, угнетение иммунных реакций, расстройства витаминного и электролитного обменов и т.п.
Часто побочные реакции, имеющие сходные клинические признаки, развиваются в результате воздействия различных причин. Например, диарея может быть следствием прямого воздействия препарата на слизистую оболочку или нервно-мышечный аппарат кишечника, но может явиться проявлением суперинфекции или дисбактериоза лекарственного генеза. Такие проявления побочных реакций на лекарства. как агранулоцитоз, гипопластическая анемия могут быть следствием токсического действия лекарственного препарата и они дозозависимы, но в их основе могут быть и реакции сенсибилизированных элементов крови и кроветворных органов с вновь возникающими антигенами, образующимися при связывании лекарственного вещества с белками плазмы крови, т.е. аллергического характера. Следовательно, деление побочных реакций на группы достаточно условно.
Антибиотики. Фармацевтическая промышленность нашей страны выпускает около 40 антибиотиков и свыше 200 лекарственных форм, приготовленных на основе антибиотиков. Переход России на рыночную экономику значительно расширил список антибактериальных препаратов, поступающих в аптеки.
Не существует ни одного антибиотика, не оказывающего в том пли ином размере побочных реакций и осложнений. По данным Всесоюзного центра по изучению побочного действия лекарственных средств на долю антибиотиков приходится 37,2 % всех лекарственных осложнений.
Уже в первые годы их применения в литературе появились единичные сообщения о побочных осложнениях, количество, частота и тяжесть которых значительно возросли за последние годы. К этому привело нерациональное, порой бесконтрольное применение антибиотиков, особенно пенициллина. По данным L. Garrodi (1976), в США 95 % лиц, получавших антибиотики, не имели показаний к их применению. Эта тенденция сохранилась и четверть века спустя спустя [Seeger J.D. et al., 1998; Leape L.L., et al., 1995, 1999; Friedman M.A. et al., 1999; Nau D.P. et al., 1997, 2000].
Переоценка действия антибиотиков привела к значительному злоупотреблению ими, распространению самолечения при малейших кишечных расстройствах, легких катаральных явлениях вирусной этиологии, при которых антибиотики не оказывают лечебного эффекта, а лишь приводят к гиперчувствительности организма. В связи с этим довольно большая часть населения в настоящее время сенсибилизирована антибиотиками. А. Д. Адо и соавт. (1970), изучая аллергические реакции при пенициллинотерапии, выявили их у 88,3% больных, повторно применявших данный препарат, 11,7 % больных с аллергическими осложнениями получали его впервые.
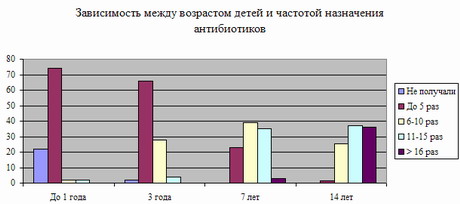
Препараты группы средств этиотропной терапии бактериальных, вирусных и паразитарных заболеваний занимают одно из ведущих мест в развитии осложнений и побочных реакций в медикаментозной терапии. Треть осложнений от этих препаратов вызвана антибиотиками, так как именно они находят наиболее широкое применение среди других лекарственных веществ. Так, по нашим данным в крупном городе к 7 годам нет ни одного ребенка, не получавшего антибиотиков, причем к 14 годам треть детей имели свыше 16 эпизодов приема антибиотиков (рис. 11). На аналогичную ситуацию указывал О. В. Бароян (1975), обследовавший четверть века тому назад детей Москвы.
О том, что антибиотики занимают первое место в группе не в связи с большей по сравнению с другими этиотропными средствами возможностью к побочным реакциям, а потому что они чаще применяются, свидетельствуют результаты широкомасштабных исследований, проведенных за рубежом. Как было установлено, побочные реакции, потребовавшие госпитализации в стационар больных, лечившихся в условиях поликлиники, наиболее часты при лечении нитрофурантоином (617 на 1 000 000 больных), в то время как антибиотики в целом находятся на 5-м месте и вызывают лишь 7 % таких реакций.
Побочные реакции, развивающиеся в связи с применением антибиотиков носят в основном аллергический характер. В популяции населения у 10 % имеется генетически обусловленная предрасположенность к аллергическим и атопическим реакциям на всевозможные антигены (аллергены).

Рис. 11
Постепенная сенсибилизация наступает в результате профессионального контакта у медицинских работников и рабочих фармацевтических предприятий, занятых производством антибиотиков. Сенсибилизация может наступить и у лиц, никогда не получавших антибиотики и не имеющих с ними профессионального контакта. Небольшие дозы их могут поступать в организм человека с коровьим молоком, в виде аэрозолей в больничных помещениях, при вакцинации. Так, в 6 % молочной продукции США и в 45 % в Англии обнаружен пенициллин [К. Wicher и соавт., 1969]. Консервация пенициллином вакцин против полиомиелита в некоторых странах может служить путем сенсибилизации населения к пенициллину. Наконец, широкое применение парентерального пути введения лекарственных веществ может сенсибилизировать организм к антибиотикам, так как длительное кипячение, до 16 часов, не ликвидирует небольших количеств пенициллина в шприцах [Coleman М., Siecal В., 1955].
Многолетние наблюдения показывают, что степень тяжести аллергических осложнений не всегда зависит от дозы лекарственного препарата и способа его введения. В литературе имеются сообщения о тяжелых осложнениях типа анафилактического шока, развившихся от инъекций шприцами, только загрязненными пенициллином [Северова Е.Я., 1969; Welsh J., 1961] при применении пенициллиновой мази в слезный мешочек, аппликационной кожной пробы с антибиотиками и даже в результате вдыхания воздуха больничных помещений, содержащих пенициллин в виде аэрозолей при ингаляции в виде аэрозоля, при закапывании в нос и введении в синусы, при постановке кожной пробы на чувствительность [Лукаш Е. К., Трахтенберг С. Б., 1965; Weiss L.R., 1963].
А. С. Лопатин и соавт. (1977) дали клинико-статистический анализ побочных реакций и осложнений антибиотикотерапии за 1971–1976 гг., зарегистрированных во Всесоюзном центре МЗ СССР по изучению побочного действия лекарственных средств при активном и пассивном выявлении (табл. 26).
Таблица 26
Структура поражения органов и систем в процессе антибиотикотерапии (%)
|
Органы и системы |
Побочные реакции и осложнения антибиотикотерапии |
Среди всех зарегистрированных побочных реакций медикаментозной терапии |
|
Кожа и ее придатки
|
36,9
|
65 6
|
|
Костно-мышечная система
|
2,4
|
58,1
|
|
Соединительная ткань
|
0,014
|
20,0
|
|
Центральная нервная система
|
5,85
|
41,9
|
|
Периферическая - II -
|
0,79
|
74,6
|
|
Вегетативная - II -
|
8,7
|
43.3
|
|
Орган зрения
|
0,8
|
80,9
|
|
Орган слуха
|
0.3
|
81,5
|
|
Вестибулярный аппарат
|
4,56
|
69,5
|
|
Психика
|
4,43
|
44,7
|
|
Желудочно-кишечный тракт
|
11,2
|
55,4
|
|
Печень и желчные пути
|
1,02
|
74,7
|
|
Метаболизм и питание
|
0,07
|
3 62
|
|
Сердечно-сосудистая система
|
9,3
|
41,4
|
|
Система дыхания
|
2,69
|
43,8
|
|
Лимфатическая система
|
0,014
|
75,0
|
|
Другие органы и системы
|
9,91
|
27,0
|
Примечание. Проценты вычислены от общего числа зарегистрированных осложнений при антибиотикотерапии.
Авторы нашли, что чаще всего поражается кожа и ее придатки. По их данным, в 79.9 % осложнений лекарственная патология носила аллергический характер, в 7,05 % – токсический, у 6,03 % – токсико-аллергический и 7,22 % осложнений биологической природы. Летальный исход зарегистрирован в 0,9 % случаев.
В группу побочных эффектов антибиотиков, связанных с биологической активностью препаратов, следует отнести реакцию Яриша-Герксгеймера, инфекционно-токсический шок, которые обусловлены так называемым "токсинным ударом" в результате массивного бактериолиза. ИТШ чаще развивается при инфекциях с выраженной бактериемией (менингококцемия, брюшной тиф, лептоспироз), особенно в случаях применения антибактериальных препаратов бактерицидного действия. Развитию шока препятствуют одновременное назначение глюкокортикостероидов (пульс-терапия), проведение инфузионно-дезинтоксикационной терапии. Для предупреждения этой группы осложнений лечение больных менингококцемией рекомендуется начинать с применения препарата бактериостатического действия -– левомицетина.
Пенициллины относятся к антибиотикам бактерицидного действия и включают препараты природные, синтетические и полусинтетические. Причем, все пенициллины обладают перекрестной аллергенностью. Повышенная чувствительность на пенициллины выявляется у 1-10 % пролеченных больных, но тяжелые реакции с развитием анафилактического шока встречаются от 0,01 до 0,05 %, смерть при своевременном оказании медицинской помощи при развитии анафилактического шока наблюдается у 0,002 % больных.
В 1957 году в США был проведен опрос, которым было охвачено 29 % всех больных и удалось установить, что 10 % из них сенсибилизированы пенициллином. Чаще всего сенсибилизация развивается при местном лечении и терапии с интервалами. Частота аллергии среди взрослого населения составляет от 0,8 до 7,4 %, у детей этот показатель ниже. На долю аллергии к пенициллину приходится до 30 % всех случаев лекарственной аллергии в США.
Анафилаксия наиболее часто встречается при парентеральном введении препаратов, но может быть и при пероральном использовании. Аллергические реакции могут развиться и при первом применении пенициллина, что объясняется сенсибилизацией малыми количествами антибиотика, находящегося в молочных продуктах, материнском молоке, яйцах, рыбе, а также перекрестными реакциями с грибами, паразитирующими на коже и ногтях людей.
Помимо анафилактического шока клиника аллергопатологии на пенициллины проявляется в виде миокардита, в основе механизма развития которого лежит ГЗТ, дерматологическими вариантами в виде крапивницы, эритематозной или кореподобной сыпи. Наблюдается и уртикарная сыпь, но она не является истинной аллергией на пенициллины, наиболее часто встречается при использовании ампициллина (9 %). Нередко наблюдается макуло-папулезная сыпь, появляющаяся на 3-14 дни после начала приема препаратов, чаще сначала она локализуется на туловище и распространяется периферически. Сыпь на пенициллины у большинства больных не ярко выражена и стихает после 6-14 дней, несмотря на продолжение приема препарата. У детей сыпь при лечении ампициллином встречаются в 5-10 % случаев. Она чаще развивается у женщин, чем у мужчин. Ко-фактором развития сыпи при лечении пенициллинами являются вирусные заболевания, она встречается у 50-80% больных инфекционным мононуклеозом, которые лечились ампициллином [Anderson J.A. ,199]. Еще чаще (в 90 %) встречается макуло–папулезная сыпь у больных лимфолейкозом и в высоком проценте случаев у лиц с ретикуло-саркомой и другими лимфомами, что вполне понятно, так как характерный для этих больных иммунодефицит определяет формирование аллергопатологии, в том числе на пенициллины.
Препараты пенициллинового ряда амоксициллин и ампициллин вызывают аллергические реакции в виде крапивницы, эритемы, отека Квинке, ринита, конъюнктивита. Иногда развиваются лихорадка, боли в суставах, эозинофилия. Крайне редко развивается анафилактический шок. Аналогичную клинику аллергопатологии может вызвать бензилпенициллин. Он чаще других препаратов пенициллинового ряда вызывает анафилактический шок.
Тетрациклины по сравнению с пенициллинами значительно реже вызывают сенсибилизацию. Возможно, это в определенной степени связано с их иммунодепрессивными свойствами. Аллергические реакции на тетрациклины чаще проявляются кожными высыпаниями, зудом, лихорадкой, артралгиями, хотя и редко, но возможен анафилактического шока.
Левомицетин (хлорамфеникол) оказывает токсическое действие главным образом на систему крови и кроветворения, однако этот эффект наблюдают только при длительном применении препарата. Наиболее серьезное осложнение - необратимая апластическая анемия, приводящая к летальному исходу, причем может развиться на терапевтические дозы препарата.
Полимиксины могут оказывать нефро- и нейротоксическое, а также при парентеральном применении - местнораздражающее действие. Нефротоксическое действие полимиксинов обусловлено повреждением клубочкового аппарата почек и характеризуется альбуминурией, гематурией, набуханием и дистрофией канальцевых клеток. В большинстве случаев эпителий почечных канальцев полностью восстанавливается после отмены препаратов. Нейротоксическое действие полимиксинов обычно связано с их передозировкой и проявляется атаксией, нистагмом, потерей чувствительности. Эти симптомы, как правило, быстро проходят, особенно при введении антигистаминных препаратов.
У 4 % больных вызывают реакции повышенной чуствительности к полимиксинам в виде лихорадки, макулопапулезной сыпи и других кожных реакций.
Цефалоспорины имеют общее с пенициллинами бета-лактамное ядро, что обусловливает возможность у 2-10 % больных перекрестных реакций с пенициллинами. При этом могут развиваться анафилактический шок, крапивница, ангионевротический отек, генерализованная эритема, макулопапулезная экзантема, лихорадка, эозинофилия. У людей с повышенной чувствительностью к пенициллину аллергические реакции на цефалоспорин развиваются в 5-6 раз чаще Из-за наличия перекрестных реакций с пенициллинами исключается применение этих препаратов при аллергии к пенициллину.
В.В. Рафальский (1999) изучил частоту и варианты нежелательных лекарственных реакций и взаимодействия при антибиотикотерапии инфекций мочевыводящих путей. Было установлено, что ингибиторзащищенные аминопенициллины (амоксициллин) побочные эффекты дают в 12 %, наиболее характерны нарушения со стороны желудочно-кишечного тракта (8,4 %). На цефалоспорины аллергические реакции (крапивница, отек Квинке, кореподобная сыпь, лекарственная лихорадка, эозинофилия, сывороточная болезнь, бронхоспазм, анафилактический шок) встречались реже, чем у антибиотиков пенициллинового ряда (у 1–3 % больных) и в порядке снижения риска аллергических реакций препараты расположены следующим образом: цефтриаксон > цефоперазон > цефокситин > цефтазидим > цефотаксим > цефуроксим. Выявлена высокая вероятность развития перекрестных реакций на цефалоспорины у больных с аллергией на пенициллин, она наиболее высока (10–15 %) для цефалоспоринов I поколения и минимальна (1–2 %) для препаратов III–IV поколения. Тяжелые аллергические реакции на цефалоспорины встречались крайне редко.
На антибиотики тетрациклинового ряда аллергические реакции встречаются редко и включают макуло-папулезные, кореподобные или эритематозные сыпи, эксфолиативный дерматит, множественную эритему, крапивницу, зуд, ангионевротический отек, астму, лекарственные высыпания на гениталиях и других областях, перикардит, обострение СКВ, гипертермию, головную боль и боли в суставах. Развиваются фотодерматиты в течение нескольких минут до нескольких часов после нахождения пациента на солнце и обычно исчезают в течение 1-2 часов после прекращения приема тетрациклинов. В большинстве случаев фоточувствительные реакции появляются в результате аккумуляции лекарства в коже и по сути являются фототоксическими, но могут быть и фотоаллергическими. Как правило, больные, имеющие повышенную чувствительность на один из производных тетрациклина, обладают повышенной чувствительностью на все тетрациклины. При длительном лечении тетрациклинами возможны такие побочные реакции, как лейкоцитоз, нейтропения, лейкопения, появление атипичных лимфоцитов, токсическая грануляция нейтрофилов, тромбоцитопения, тромбоцитопеническая пурпура, снижение миграции лейкоцитов и угнетение процессов фагоцитоза.
В группе макролидов чаще наблюдаются побочные реакции на эритромицин в виде холестаза, развивающегося на 10-12 дни приема препарата, а эритромицин-эстолат, кроме того, может вызвать повреждение печени.
Основной побочный эффект аминогликозидов - нейротоксическое действие, которое наиболее выражено при внутривенном введении антибиотиков и проявляется резким снижением кровяного давления и угнетением дыхания, нередко приводящим к летальному исходу. Это обусловлено угнетающим влиянием аминогликозидов на сосудодвигательный и дыхательный центры. Антибиотики этой группы в высоких концентрациях, что имеет место при быстром внутривенном введении их, обладают курареподобным и ганглиоблокирующим действием, что может привести к остановке дыхания за счет блокирования передачи импульса в нервных волокнах дыхательных мышц. При длительном использовании аминогликозиды оказывают токсическое действие на вестибулярный аппарат и VIII пару черепно-мозговых нервов, что проявляется расстройствами слуха
При парентеральном введении аминогликозиды могут повреждать клетки проксимального отдела извитых канальцев почек, в результате чего снижается клубочковая фильтрация, развиваются альбуминурии и микрогематурии. Это
побочное влияние аминогликозидов можно свести к минимуму, если избегать по возможности их внутривенного введения, а при необходимости инъекции в вену следует проводить медленно, назначать точные терапевтические дозы и не затягивать курс лечения, а также не применять антибиотики этой группы в комбинациях с другими лекарственными веществами, оказывающими нейро- и нефротоксическое действие.
Среди аминогликозидов первым и широко применяемым антибиотиком был стрептомицин. Но уже вскоре после первых лет его применения была выявлена его способность к нарушению слуха, в основе которой лежат токсические реакции. Аллергическую природу имеют лекарственная лихорадка, макуло-папулезные высыпания и эскфолиативный дерматит. Высокая частота развития аллергического контактного дерматита наблюдается у медицинского персонала и у лиц, занятых в фармацевтической промышленности.
Стрептомицин может вызывать развитие перекрестных аллергических реакций с неомицином. Некоторые аминогликозиды содержат сульфиты, обусловливающие развитие аллергических реакций, включая анафилактические. Побочные проявления приема рифампицина характеризуются поражением кожи, тромбоцитопенией, гемолитической анемией, лекарственной лихорадкой, острой почечной недостаточностью.
Антибиотики группы линкомицина (линкомицин, клиндамицин) могут вызывать аллергические реакции в виде ангионевротического отека, сывороточной болезни, анафилактического или анафилактоидного шока, но эта группа побочных эффектов встречается редко. Чаще наблюдаются реакции токсического характера в виде тошноты, рвоты, болей в эпигастрии, диареи, глоссита, стоматита, обратимой лейкопении за счет нейтропении, тромбопении.
В настоящее время среди основных химиотерапевтических средств для лечения инфекций одно из важных мест заняли фторхинолоны – большая группа высокоэффективных антимикробных препаратов с широкими показаниями к применению. Всю группу объединяет принадлежность препаратов к классу хинолонов с единым механизмом действия на микробную клетку - ингибиторы ДНК-гидразы микробов.
Нефторированные хинолоны (например, налидиксовая кислота), имеют ограниченный спектр действия с преимущественной активностью в отношении некоторых грамотрицательных бактерий, главным образом, из группы энтеробактерий. Особенности фармакокинетики нефторированных хинолонов позволяют применять эти препараты при чувствительном возбудителе только для лечения инфекций мочевыводящих путей и некоторых кишечных инфекций. Быстрое развитие лекарственной резистентности к нефторированным хинолонам у бактерий существенно ограничивает их применение в клинике. Нитроксолин (син. 5-нитрокс, 5-НОК), относящийся к производным 8-оксихинолона в связи со случаями тяжелых побочных реакций в большинстве стран запрещен, хотя у нас по прежнему входит в группу современных лекарственных средств [Крыжановский С.А., Вититнова М.Б., 2000] и широко используется при инфекциях мочеполовой системы. При лечении им наиболее часты отрицательными эффектами в виде головной боли, головокружения, диспепсических расстройств, аллергических реакций, частота последних достигает 5,1 % . Среди тяжелых побочных реакций при лечении 5-НОК развиваются периферические полиневриты, проявляющиеся парестезиями и прогрессирующей параплегией, и атрофия зрительного нерва, которая может приводить к полной потере зрения. Эти нарушения могут сочетаться с церебральными расстройствами: заторможенностью, ретроградной амнезией.
Группу фторхинолонов представляют монофторхинолоны – ципрофлоксацин, офлоксацин, пефлоксацин и норфлоксацин и дифторхинолон ломефлоксацин, зарегистрированные и разрешены для применения в России. За рубежом, кроме того, применяются эноксацин, спарфлоксацин, флероксацин, суфлоксацин, руфлоксацин.
При приеме препаратов этой группы у 1 % больных встречаются слабовыраженные кожные высыпания в сочетании с эозинофилией, кожным зудом, крапивницей, кожным кандидозом, гиперпигментацией, ангионевротическим отеком, отеками лица, губ, век, развитием конъюнктивита. Кроме того, возможно развитие сердечно-сосудистого коллапса, парестезии, отека гортани и лица, крапивницы. Ципрофлоксацин противопоказан больным, имеющим в анамнезе аллергию на другие хинолоны.
Обобщенные данные наиболее характерных побочных реакций антибиотикотерапии представлены в табл.27.
Таблица 27
Наиболее распространенные побочные эффекты антибиотикотерапии
|
Группы антибиотиков |
Нежелательные эффекты |
| Пенициллины | Аллергические реакции ( анафилактический шок) Реакция Яриш- Герксгеймера, инфекционно-токсический шок) |
| Цефалоспорины | Аллергическая реакция (анафилактический шок) Гематологическая реакция (анемия, лейкопения) Нарушения функции печени (гипопротромбинемия, трансфераземия) Нефротоксичность |
| Аминогликозиды | Ототоксичность (нарушение функции вестибулярного и
кохлеарного аппаратов) Нефротоксичность, нервно-мышечная блокада |
| Хинолоны (фторхинолоны) | Гематологические реакции (цитопения, гемолитическая анемия)
Гематотоксичность Возбуждение ЦНС (повышение судорожного порога) Диспептические расстройства (дисбактериоз) |
| Тетрациклины |
Гепатотоксичность Нефротоксичность Диспептические расстройства (дизбактериоз) Гематологические изменения и вазопатия у детей до 8-летнего возраста |
| Макролиды |
Диспептические расстройства (стимуляция моторики ЖКТ) Гепатотоксичность |
|
Линкосамиды |
Диспептические расстройства Псевдомембранозный колит Гепатотоксичность Нефротоксичность |
| Полимиксины |
Выраженная нефротоксичность Нейротоксичность Нервно-мышечная блокада Тромбоцитопения Гипокальциемия Гипокалиемия |
| Гликопептиды (ванкомицин) | Аллергические реакции Панцитопения Ототоксичность Нефротоксичность Гепатотоксичность Флебиты, тромбофлебиты |
| Хлорамфеникол (левомицетин) | Гематотоксичность (агранулоцитоз, апластическая анемия и
др.) Нейротоксичность (возможное поражение зрительного нерва) |
| Рифампицин |
Гепатотоксичность Гематотоксичность (гемолитическая анемия, тромбоцитопения) |
Производные нитрофурана. Как уже отмечалось выше, производные нитрофурана, в частности нитрофурантоин занимает первое место среди лекарственных препаратов из группы противомикробных средств, давших побочные реакции при амбулаторном лечении и потребовавших госпитализацию больных.
При применении нитрофурантоина наиболее часты желудочно-кишечные расстройства (тошнота, рвота), поражения печени, периферической нервной системы, лекарственная лихорадка, аллергические реакции в виде кожных сыпей, анафилаксии, аллергической патологии легких, гематологические расстройства. Причем тяжелая патология легких на уровне критического состояния встречалась с частотой 1 случай на 5000 больных при проведении одного курса терапии и 1 случай на 716 пациентов при проведении 10 курсов и более. Для легочной патологии у этих больных наиболее характерны одышка, кашель с мокротой или без нее, лихорадка, бронхоспазм, а также миалгия, эозинофилия. При обследовании в легких выявлялись лобарная инфильтрация, плевральный выпот, интерстициальное воспаление, васкулиты.
Поражения носят обратимый характер, инволюция клиники идет быстро после отмены препарата. Как полагают, патогенез этого вида патологии аллергический.
Нитрофурантоин также является одной из наиболее частых причин лекарственного гепатита, особенно у пожилых людей, преимущественно хронического течения. Обусловлен гепатит некрозом гепатоцитов, реже развиваются холестатические и смешанные поражения печени.
Для гематотоксических реакций, развивающихся на нитрофурантоин, чаще всего развивается острая гемолитическая анемия, она характерна для лиц с дефицитом глюкозо-6-фосфатдегидрогеназы в эритроцитах и встречается с частотой 1 случай на 100 000 назначений препарата. Изредка развиваются мегалобластная анемия, агранулоцитоз, тромбоцитопения, лейкопения.
Сульфаниламиды являются малотоксичными соединениями, но при повышенной чувствительности организма, чрезмерном увеличении дозировки или длительном курсе лечения они также могут вызывать побочные явления, главным образом в системе кроветворения и почках. Патология со стороны кроветворной системы, вызванная сульфаниламидами, характеризуется явлениями анемии, цианоза, метгемоглобинемии, лейкопении, агранулоцитоза, уменьшением количества гемоглобина. При высоких дозах и при длительном применении под влиянием сульфаниламидов вначале уменьшается количество лейкоцитов, главным образом за счет сегментоядерных, затем уменьшается количество гемоглобина, понижается резистентность эритроцитов, появляется метгемоглобин. Наиболее сильно изменяется состав крови под влиянием стрептоцида, норсульфазола.
Так как сульфаниламиды выводятся из организма главным образом почками, концентрация их в почке часто превышает пределы растворимости и препараты выкристаллизовываются в осадок. Появлению кристаллурии и связанных с ней почечных осложнений способствуют высокая концентрация препарата в моче, уменьшение диуреза, кислая реакция мочи.
Довольно частыми симптомами побочных эффектов сульфаниламидов являются контактный дерматит, экзантемы, фоточувствительный дерматит, лекарственная лихорадка и изменения картины крови.
Метаболизируются сульфаниламиды печеночным ацетилированием и цитохромом Р-450, поэтому люди с наследственно медленным типом ацетилирования более склонны к развитию аллергии на эти препараты. Причем печень может служить органом - мишенью для развития лекарственной аллергии. Поражения печени, индуцированные лекарственными средствами, можно подразделить на гепатоцеллюлярные, холестатические, сосудистые и смешанные. Поражение печени под влиянием сульфаниламидов проявляется желтухой, повышением активности трансаминаз и другими характерными для острого гепатита симптомами. В этих случаях подозрение на лекарственную аллергию может возникнуть при сочетании лекарственного поражения печени с сыпью, эозинофилией и лихорадкой. После отмены препарата состояние, как правило, нормализуется в течение 2-х недель. Течение и прогноз лекарственного гепатита чаще всего благоприятный, но описаны случаи острого некроза печени, заканчивающиеся летальным исходом.
Аллергические реакции на сульфаниламиды в значительной степени зависят от состояния иммунной системы. Так, макуло-папулезные высыпания встречаются у 3 % больных, использующих сульфамиды и у более чем у половины ВИЧ - инфицированных.
В связи с серьезными побочными эффектами сульфаниламиды противопоказаны пациентам, имеющим в анамнезе повышенную чувствительность на любые противовоспалительные сульфамиды, а также на некоторые диуретики - такие, как, например, ацетазоламид и тиазиды противодиабетические производные сульфанилмочевины. Сульфасалазин противопоказан пациентам с повышенной чувствительностью к салицилатам.
Антиретровирусные препараты. ВИЧ-инфекция в России, как и в мире в целом, продолжает набирать темпы. Показатель заболеваемости на май 2000 года составил 3 на 100 000 населения, что в 10 раз выше, чем заболеваемость брюшным тифом, выше показателей заболеваемости риккетсиозами, дифтерией, корью, иерсиниозом, примерно такая же, как заболеваемость менингококковой инфекцией, клещевым энцефалитом. Эпидемия в 2000 году в стране набирала темпы и к сентябрю показатель заболеваемости уже составил 10 на 100 000. Так как в основном ВИЧ-инфицированные – это больные наркоманией, внутривенно получающие наркотики, темпы прогрессирования болезни у них выше и уже через 3-5 лет мы в праве ожидать значительный рост больных в стадии пре-СПИДа и СПИДа, т.е. требующей медикаментозного лечения и не только антиретровирусными препаратами, но и лечения суперинфекций, определяющих клинику ВИЧ-инфекции в целом.
Все это свидетельствует о необходимости незамедлительно решать проблему пожизненной дорогостоящей терапии миллионов людей в мире и тысяч – в нашей стране.
Целью терапии больных ВИЧ-инфекцией является максимальное и продолжительное угнетение репликации вируса, восстановление и/или сохранение функции иммунной системы, улучшение качества жизни, снижение связанной со СПИДом заболеваемости и смертности. На сегодняшнем уровне это может быть достигнуто максимальным соблюдением назначенной схемы антиретровирусной терапии, рациональной последовательностью применения препаратов, сохранением резервных схем лечения и препаратов на будущее.
Хотя терапия ВИЧ-инфекции остается сложнейшей и нерешенной проблемой, определенные успехи, безусловно, имеют место. О наметившихся сдвигах эффективности лекарственной терапии уже в первые годы пандемии свидетельствуют следующие данные: в 1986 году свыше 70 % инфицированных в ближайшие 2 года заболели СПИДом или умерли, а среди инфицированных в 1989 году - лишь 20%. ибо в практику лечения больных был внедрен первый антиретровирусный препарат – азидотимидин, ставший базисным для всех последующих схем комбинированной терапии.
Сегодня арсенал лекарственных средств позволяет подавить вирусную репликацию у большей части больных на определенный, иногда довольно длительный срок, перевести заболевание в хроническое течение. Но, тем не менее, терапией удается лишь продлить жизнь больного и нет возможности полностью остановить инфекционный процесс. По мнению Люка Монтанье (1999) мы научились лечить лишь суперинфекции ВИЧ/СПИД, но не сам СПИД.
Для успешного лечения больных необходимо решение следующих вопросов: 1) наличие химиотерапевтических средств, направленных непосредственно на ВИЧ, 2) наличие лекарственных препаратов, направленных на ту паразитарную, бактериальную, вирусную, протозойную или грибковую суперинфекцию, в том числе онкопатологию, которая у конкретного больного определяет клинику болезни, 3) коррекция лекарственными средствами иммунодефицита.
Теоретически разработка этиотропной терапии ВИЧ-инфекции базируется на ряде принципиальных подходов (табл. 28):
1) блокада лиганд вируса и в первую очередь gp 120 и gp 41 антилигандами, в частности анти gp120 и gp 41 – антителами;
2) создание препаратов, имитирующих рецепторы CD4, которые бы связывались с лигандами вируса и блокировали его возможность соединяться с клетками человека;
3) блокада ферментных систем, обеспечивающих репликацию вируса в клетке-мишени: а) ингибиторы протеаз, осуществляющих “раздевание” вируса, проникшего в цитоплазму клетки-мишени, б) ингибиторы обратной транскриптазы, обеспечивающей транскрипцию РНК вируса в ДНК, в) ингибиторы интегразы, обеспечивающей объединение ДНК вируса с ДНК клетки, г) ингибиторы Н-РНК-азы, обеспечивающей деградацию нитей РНК вириона, 4) ингибиторы регуляторных генов tat и rev, нарушающих транскрипцию,
Таблица 28
Жизненный цикл ВИЧ и антиретровирусные препараты
|
Фазы |
Обеспечение |
Лекарственные препараты |
|
1. Связывание вириона с мембраной |
gp120 CD4 |
отсутствуют |
|
2.Инъекция содержимого капсида ВИЧ в клетку |
отсутствуют |
|
|
3.Обратная транскрипция с образованием провирусной ДНК
|
Траснкриптаза |
Нуклеозидные и ненуклеозидные ингибиторы обратной транскриптазы |
|
4.Интеграция провирусной ДНК в ДНК клетки-мишени |
Интеграза |
отсутствуют |
|
5.Транскрипция вирусных полипептидов в хромосомном наборе хозяина |
отсутствуют |
|
|
6.Трансляция и рассечение вирусных полипептидов на функционирующие белки |
Протеаза |
Ингибиторы протеазы |
|
7.Сборка вирусов и выход из клетки |
отсутствуют |
трансляцию и рассечение вирусных белков; 5) ингибиторы посттрансляционных процессов, а именно гликолизирования и миристилирования белков.
Сегодня с учетом жизненного цикла вируса созданы препараты, ингибирующие обратную транскриптазу и протеазу. До 1991 года из лекарственных препаратов, непосредственно действующих на ВИЧ, использовался только азидотимидин (фирма Glaxo Wellcome” выпускает его под названием зидовудин, ретровир, в нашей стране торговое название препарата – тимозид). Азидотимидин (АЗТ) – нуклеозид, ингибитор обратной транскриптазы. Он был создан в 1964 году для лечения онкологических больных. С 1987 года стал применяться при лечении ВИЧ-инфекции, так как за счет ингибирования обратной транскриптазы тормозит репликацию ВИЧ-1, ВИЧ-2, других ретровирусов и вируса Эпштейна – Барр. Уже первые годы применения азидотимидина в терапии больных позволили снизить летальность, а число суперинфекций уменьшилось в 5 раз, более замедленными темпами развивалась CD4+ лимфопения, у больных нарастала масса тела.
К недостаткам терапии азидотимидином следует отнести в первую очередь формирование более, чем у половины больных устойчивых штаммов вирусов при приеме препарата свыше 6 мес., при этом прослеживается взаимосвязь формирования устойчивости с фазой болезни: при назначении в ранние сроки болезни устойчивость формируется реже, чем в более поздние фазы. Вновь сформировавшиеся резистентные штаммы порой более агрессивны, чем исходный вариант вируса. Накопленный опыт более чем десятилетнего применения азидотимидина поставил перед клиницистами вопрос, чего больше при монотерапии больных азидотимидином или любым другим антиретровирусным препаратом - пользы или вреда. При терапии этими весьма токсичными препаратами в виде монотерапии быстро развивается устойчивость вируса к ним, противовирусное действие его прекращается, а токсическое продолжается [Ayers K.M. et al., 1996; White A. et al., 1997;. Wang Y. et al., 1999]. Очевидно, при монотерапии больше все же вреда.
Проблема, насколько важно усовершенствование методик лечения больных, возникла в 1996 году, когда за рубежом был внедрен в широкую практику тест оценки вирусной нагрузки на плазму – полимеразную цепную реакцию (ПЦР), позволившую прогнозировать прогрессирование болезни. Внедрение новых антиретровирусных препаратов и возможность оценки вирусной нагрузки на плазму позволили сформулировать задачу антиретровирусной терапии - снижение вирусной нагрузки до неопределяемого с помощью ПЦР уровня, т.е. ниже 50 копий/мл, так как при такой нагрузке прекращается разрушение иммунной системы вирусом, предотвращающее развитие суперинфекций, значительно падает угроза формирования резистентных штаммов вируса, хотя репликация последнего не прекращается.
Помимо АЗТ среди аналогов нуклеозидов с активностью против обратной транскриптазы нашли широкое применение диданозин (видекс, ddI, 1991), зальцитабин (хивид, ddC, 1992), ставудин (1994), ламивудин (1995), еще позже появились адефовир, ладанозин (фтористый аналог диданозина), FTC (фтористый аналог ламивудина с более выраженной активностью). Широко в клиническую практику внедрены ненуклеозидные аналоги с активностью против обратной транскриптазы: делавирдин (рескриптаза) и невирапин (вирамун). С 1995-1996 гг. также внедрены ингибиторы протеазы: индинавир, саквинавир, ритонавир, нелфинавир. Пополнился список ненуклеозиных аналогов, по активности не уступающих эффекту ингибиторам протеазы. Как видно из таблицы 29, 1995-1997 г.г. были наиболее плодотворными по внедрению в клиническую практику новых лекарственных препаратов с антиретровирусной активностью и для лечения суперинфекций ВИЧ/СПИД (до 10. 99).
Таблица 29
Этапы достижений в терапии больных ВИЧ-инфекцией
|
Год |
Лекарственные препараты |
|
1995 год: |
Мепрон - для лечения пневмоцистной пневмонии Саквинавир – 1-й ингибитор протеазы Фоскарнет – для лечения герпеса Цидофовир – для лечения CMV-инфекции Кларитромицин - для лечения атипических микобактериозов Ганцикловир – для лечения СМV-инфекции Доксил - для лечения саркомы Капоши Эпивир (ламивудин, ЗТС) – ингибитор обратной транскриптазы, рекомендован для комбинированного лечения Амфотерицин В – для лечения аспергиллеза Саквинавир (инвиразе, фортовазе) – ингибитор протеазы Ставудин (зерит, d4T)– ингибитор протеазы, рекомендован для лечения больных, ранее получавших АЗТ |
|
1996 год: |
Ритонавир (норвир) – ингибитор протеазы, рекомендован для комбинации с ингибиторами обратной транскриптазы Ганцикловир – для лечения CMV-ретинита Криксиван (индинавир)– ингибитор протеазы, рекомендован один или в комбинации Даунорубицин – для лечения саркомы Капоши Азитромицин – для лечения атипических микобактериозов Невирапин – ненуклеозидный ингибитор обратной транскриптазы Цидофовир – для лечения CMV-ретинита |
|
1997 год: |
Интраконазол – для орофарингита и эзофагита кандидозного Нелфинавир (вирацепт) – 1-й ингибитор протеазы, разрешенный для подростков Ритонавир – разрешен для лечения подростков Делавирдин (рескриптор) – 1-й из ненуклеозидных ингибиторов обратной транскриптазы, рекомендованный в комбинации Сообщено о гиперглицемии при лечении ингибиторами протеазы Токсол – для лечения саркомы Капоши Фамвир – для лечения рецидивирующего генитального герпеса Комбивир - комбинация азидотимидин/эпивир с приемом 2 раза в день Фортовазе – новая форма саквинавира |
|
1998 год: |
Фамвир (фамцикловир) – для лечения рецидивирующего герпеса Ифавиренц (сустива) –ненуклеозидный ингибитор обратной транскриптазы Зиаген (абакавир) – нуклеозидный ингибитор обратной транскриптазы, рекомендован для лечения взрослых и детей |
|
1999 год: |
Панретин – мазь для лечения саркомы Капоши иммуномодулирующий препарат "РЕМУН", эффективно активирует Т-клетки, которые, в свою очередь, инактивируют вирус иммунодефицита и возбудителей суперинфекций ВИЧ/СПИД (CDC, 2000). Агенеразе (ампренавир) – ингибитор протеазы. |
При назначении лекарственных препаратов больному ВИЧ-инфекцией происходит обоюдное взаимодействие между вирусом, лекарственным препаратом и организмом человека (рис. 12).
Взаимодействия при лечении ВИЧ-инфекции
Рис. 12
Антиретровирусный эффект нуклеозидных ингибиторов обратной транскриптазы можно проследить на примере АЗТ. При приеме внутрь азидотимидин хорошо всасывается, период полувыведения составляет 3-4 ч, выводится через почки. Терапия предусматривает пожизненный пероральный прием.
Азидотимидин по структуре близок к нуклеозиду тимидину, входящему в состав ДНК. В клетке азидотимидин подвергается ферментативному фосфорилированию с образованием азидотимидина трифосфата, являющегося активной формой препарата, так как азидотимидинтрифосфат является аналогом тимидинтрифосфата - одного из мономеров ДНК. Механизм подавления синтеза вирусной ДНК, очевидно, состоит в конкурентном ингибировании и терминации синтеза цепи ДНК. Под конкурентным ингибированием понимается связывание азидотимидинтрифосфата с обратной транскриптазой в том участке, который в норме связывает обычные нуклеозидтрифосфаты. Терминация синтеза цепи ДНК - обратная транскриптаза ошибочно включает азидотимидинтрифосфат в растущую цепь вирусной ДНК вместо тимидинтрифосфата, но присоединение следующего нуклеотида невозможно, так как в молекуле азидотимидинтрифосфата нет гидроксильной группы, которая необходима для образования связи со следующим нуклеотидом. Вирус не в состоянии исправить эту ошибку и синтез ДНК прекращается.
Отличительной чертой всех антиретровирусных препаратов, в том числе ингибиторов обратной транскриптазы является их высокая токсичность. Характеристика побочных реакций основных ингибиторов обратной транскриптазы представлена в табл. 30.
Таблица 30
Характеристика побочных реакций нуклеозидных ингибиторов обратной транскриптазы (НИ ОТ)
|
Название Торговое название |
Зидовудин (АЗТ, ЗДВ) "Ретровир" |
Диданозин (ddi) "Видекс" |
Зальцитабин (ddc) "Хивид" |
|
Влияние приема пищи |
Прием лекарства не связан с приемом пищи |
Принимать за 1/2 ч до или через 1 ч после еды |
Прием лекарства не связан с приемом пищи |
|
Побочные реакции |
Угнетение костного мозга: Анемия и/или нейтропения. Субъективные жалобы: симптомы со стороны ЖКТ, головная боль, бессонница, астения. Ацидоз и стеатоз при лечении НИ ОТ наблюдаются редко, но могут угрожать жизни больного. |
Панкреатит Периферические невриты Тошнота Диарея Ацидоз и стеатоз при лечении НИ ОТ наблюдаются редко, но могут угрожать жизни больного. |
Периферические невриты Стоматит
Ацидоз и стеатоз при лечении НИ ОТ наблюдаются редко, но могут угрожать жизни больного. |
Продолжение таблицы 30
|
Название Торговое название |
Ставудин (d4Т) "Зерит" |
Ламивудин (3ТС) "Эпивир" |
Абакавир (АВС) "Зиаген" |
|
Влияние приема пищи |
Прием лекарства не связан с приемом пищи |
Прием лекарства не связан с приемом пищи |
Прием лекарства не связан с приемом пищи Алкоголь на 41% снижает концентрацию |
|
Побочные реакции |
Периферические невриты Ацидоз и стеатоз при лечении НИ ОТ наблюдаются редко, но могут угрожать жизни больного |
(Минимальная токсичность) Ацидоз и стеатоз при лечении НИ ОТ наблюдаются редко, но могут угрожать жизни больного |
Реакция гиперчувствительности: лихорадка, сыпь, тошнота, рвота, слабость, анорексия (иногда с летальным исходом); Ацидоз и стеатоз при лечении НИ ОТ наблюдаются редко, но могут угрожать жизни больного * |
* Если у больного появились симптомы или признаки гиперчувствительности, лечение абакавиром следует немедленно прекратить и не следует предпринимать попытку возобновления лечения абакавиром, так как через несколько часов вновь появятся признаки гиперчувствительности и может наблюдаться летальный исход.
К недостаткам этих препаратов, как показал накопленный клинический опыт, относятся: а) не полностью подавляют репликацию вируса, б) высокая токсичность, в том числе азидотимидина на костный мозг, диданозина – нейротоксический эффект и способность вызвать тяжелый геморрагический панкреатит. Наиболее часто побочные эффекты проявляются анемией, поражением желудочно-кишечного тракта, неврологической симптоматикой, сыпью. К недостаткам всей группы ингибиторов обратной транскриптазы относятся быстрое формирование мутантных форм вируса с появлением у последних резистентности к этим лекарственным препаратам.
Вторую группу антиретровирусных препаратов представляют ненуклеозидные ингибиторы обратной транскриптазы. Характеристика побочных эффектов препаратов этой группы представлена в табл. 31.
Таблица 31
Характеристика ненуклеозидных ингибиторов обратной транскриптазы (ННИ ОТ)
|
Название Торговое название |
Невирапин "Вирамун" |
Делавирдин "Рескриптор" |
Ифавиренц "Сустива" |
|
Влияние приема пищи |
Прием лекарства не связан с приемом пищи |
Прием лекарства не связан с приемом пищи |
Избегать принимать лекарство после жирной пищи, так как концентрация на 50% падает |
|
Побочные реакции |
Сыпь* Повышение уровней трансаминаз Гепатит |
Сыпь* Повышение уровней трансаминаз Головные боли |
Сыпь* Симптомы со стороны ЦНС** Повышение уровней трансаминаз Тератогенность (для обезьян) |
Во время клинических испытаний из-за появления сыпи прием ненуклеозидных ингибиторов обратной транскриптазы (ННИ ОТ) пришлось прекратить у 7 % получавших невирапин, 4,3 % – делавирдин и 1,7 % больных, получавших ифавиренц.
** В том числе головокружение, сонливость, бессонница, спутанность сознания, нарушения концентрации, амнезия, возбуждение, деперсонализация, галлюцинации и эйфория. Общая частота этих симптомов при приеме ифавиренца составила 52 % (26 % в контрольной группе); 2,6 % больных вынуждены прекратить лечение ифавиренцем из-за этих симптомов.
К недостаткам терапии ингибиторами обратной транскриптазы относится и то обстоятельство, что они преимущественно действуют на популяцию остро инфицированных клеток и не эффективны на популяцию латентно-инфицированных вирусом клеток организма, в этой фазе инфекции эффективных ингибиторы протеазы.
Самую терапевтически эффективную и самую токсичную группу антиретровирусных препаратов представляют ингибиторы протеазы [Eastone J.A., Ltcker C.F., 1997; Visnegarwala F. et al., 1997; Carr A. et al., 1999]. Ингибиторы протеазы, проникая в инфицированные вирусом клетки, блокируют активность вирусного фермента протеазы, препятствуют распаду длинных цепей протеинов и энзимов на короткие звенья, необходимые ВИЧ для образования новых копий. Без них вирус дефектен и не может инфицировать клетку. Ингибиторы протеазы более мощно тормозят репликацию вируса, чем ингибиторы обратной транскриптазы и за 1 мес. лечения снижают вирусную нагрузку на 99 %, в силу чего наступает ремиссия болезни, повышается уровень CD4+ лимфоцитов. Действие ингибиторов протеазы осуществляется в лимфоидных клетках человека. Поскольку протеаза ВИЧ отличается от протеазы человека, ингибиторы вирусной протеазы действуют избирательно, не блокируя функцию фермента клеток человека. Но к этим препаратам и быстрее формируются устойчивые клоны вирусов, особенно при использовании ингибиторов протеаз в виде монотерапии.
Среди ингибиторов протеазы (табл. 32) наиболее широкое распространение получили криксиван и инвираза в связи с низкой связываемостью с белками плазмы, а, следовательно, возможностью в активной форме в больших концентрациях накопиться в плазме, а также способностью проникать через гематоэнцефалический барьер.
Таблица 32
Характеристика ингибиторов протеазы (ИП)
|
Название Торговое название |
Индинавир "Криксиван" |
Ритонавир "Норвир" |
Нельфинавир "Вирацепт" |
|
Влияние приема пищи |
Принимать за 1 час до или через 2 часа после приема пищи Можно принимать с обезжиренным молоком или нежирной пищей |
Принимать, по возможности, вместе с пищей - это может повысить толерантность к лекарству |
Принимать с пищей |
|
Хранение |
При комнатной температуре |
Капсулы - в холодильнике Оральный раствор не хранить в холодильнике |
При комнатной температуре |
|
Побочные реакции |
Почечнокаменная болезнь Симптомы ЖКТ, тошнота Повышение непрямого билирубина А также: головная боль, астения, нарушение зрения, головокружения, сыпь, металлический привкус во рту, тромбоцитопения Гипергликемия* Перераспределение жировой клетчатки и нарушение липидного обмена** |
Симптомы со стороны ЖКТ, тошнота, рвота, диарея Парестезии Гепатит Астения Нарушения вкуса Лабораторно: повышаются >200% триглицериды, трансаминазы Гипергликемия* Перераспределение жировой клетчатки и нарушения липидного обмена** |
Диарея Гипергликемия* Перераспределение жировой клетчатки и нарушения липидного обмена**
|
* Усугубление нарушений углеводного обмена у больных диабетом и новые случаи диабета
** С приемом ингибиторов протеазы связана липодистрофия. Оценивать риск заболеваний сердечно-сосудистой системы. Может потребоваться диета, лекарственное снижение липидов, прекращение приема ингибитора протеазы (ИП).
Продолжение таблицы 32
| Название Торговое название |
Саквинавир | Ампренавир "Агенераза" |
|
| "Инвираза" | "Фортоваза" | ||
| Влияние приема пищи | Прием пищи не оказывает влияния, если инвиразу принимают с ритонавиром | Принимать с большим количеством пищи | Можно принимать с нежирной пищей |
| Хранение | При комнатной температуре | В холодильнике или при комнатной температуре (до 3 месяцев) |
При комнатной
температуре |
| Побочные реакции | Симптомы ЖКТ, тошнота и диарея
Головная боль Трансаминазы Гипергликемия* Перераспределение жировой клетчатки и нарушение липидного обмена** |
Симптомы со стороны ЖКТ, тошнота,
диарея, боли в животе и диспепсия
Головная боль Трансаминазы Гипергликемия* Перераспределение жировой клетчатки и нарушения липидного обмена** |
Симптомы со стороны ЖКТ, тошнота,
рвота, диарея
Сыпь Парестезии слизистых оболочек рта Гипергликемия* Перераспределение жировой клетчатки и нарушения липидного обмена** |
* Усугубление нарушений углеводного обмена у больных диабетом и новые случаи диабета
** С приемом ингибиторов протеазы связана липодистрофия. Оценивать риск заболеваний сердечно-сосудистой системы. Может потребоваться диета, лекарственное снижение липидов, прекращение приема ингибиторов протеазы.
Токсичность ингибиторов протеазы довольно выражена, у больных через 1-2 года терапии развивается липодистрофия и растет холестерин крови. Отрицательные метаболические эффекты ингибиторов протеазы значительно снижают эффект терапии.
Так как ингибиторы протеазы обладают выраженными побочными эффектами, идет поиск схем, которые бы не включали ингибиторы протеазы, а состояли из трех нуклеозидных аналогов, в частности начинают применять комбинации трех ингибиторов обратной транскриптазы, в каждую включается новый сильный нуклеозидный аналог абакавир (циаген). Другие схемы включают ненуклеозидные ингибиторы обратной транскриптазы ифавиренц и невирапин (вирамун). Имеется определенный опыт применения гидроксимочевины (Hydroxyurea), как антиретровирусного препарата. Она была синтезирована против рака, но стала также использоваться в комбинации с диданозином или другим антиретровирусным препаратом и может на длительное время снизить вирусную нагрузку на плазму. Но так как гидроксимочевина токсична для костного мозга, она не может быть использована в комбинации с азидотимидином.
Некоторые нуклеозидные аналоги не должны применяться вместе, например, азидотимидин со ставудином или диданозин с зальцитабином. Нельзя в комбинацию включать одновременно лекарственные средства, имеющие одно основание, например ddC и 3ТС (совпадение по последнему знаку). Если вирус резистентен к одному лекарственному препарату определенного класса, то он резистентен и к другим препаратам этого класса - перекрестная резистентность. Поэтому при необходимости изменения вида терапии из-за неэффективности применяемого комплекса заменяют все лекарственные препараты. Если больной не ответил положительным эффектом на 2-3 комбинации, возможности воздействия на патологический процесс можно считать исчерпанными.
При проведении активной антиретровирусной терапии необходимо учитывать некоторые примечания (табл. 33). Не рекомендуется одновременное назначение некоторых лекарств вместе с антиретровирусными препаратами (табл. 34).
Таблица 33
Примечания при приеме некоторых препаратов
|
Препарат |
Примечания |
|
Делавирдин мезилат |
Необходимо принимать по крайней мере за 1 ч до приема пищи |
|
Ифавиренц |
Избегать очень жирной пищи, предпочтительно принимать перед сном. Возможны побочные эффекты со стороны ЦНС |
|
Невирапин |
Первые 2 недели терапии по 1 табл. (200 мг) в день |
|
Диданозин |
Прием натощак. Алкоголь может усилить токсич- ность. Для больных массой < 60 кг доза 125 мг 2 раза в день |
|
Ламивудин/ зидовудин |
Комбинацию нельзя назначать больным, нуждающимся в коррекции дозы |
|
Ставудин |
Для больных массой < 60 кг по 30 мг 2 раза в день |
|
Ампренавир |
Исключить очень жирную пищу. |
|
Индинавир |
Ежедневно выпивать не менее 1,5 л жидкости |
|
.Ритонавир |
Дозу повышать в течении 2 недель: 1-2 день - по 300 мг 2 раза в день 3-5 день - по 400 мг 2 раза в день 6-13 день - по 500 мг 2 раза в день с 14 дня - по 600 мг 2 раза в день |
Применение антиретровирусных препаратов и других лекарственных средства одновременно назначаемых против конкретных суперинфекций часто вызывает органопатологию:
– Панкреатит – динанозин, ставудин, пентамидин, зальцитабин, ламивудин (у детей);
– Дисфункцию почек – адефовир, аминогликозиды, цидофовир, фоскарнет, амфотерицин В (амфотекс);
– Супрессию костного мозга – зидовудин, ганцикловир, триметоприм/сульфаметоксазол, интерферон-альфа, триметрексат;
– Периферическую нейропатию – ставудин, диданозин, зальцитабин;
– Сыпь – ифавиренц, невирапин, делавирдин, абакавир, ампренавир.
Таблица 34
Лекарства, которые не рекомендуется применять вместе с антиретровирусными препаратами
|
Группа лекарств |
Индинавир |
Ритонавир * |
Саквинавир |
Нельфинавир |
Ампренавир |
|
Блокаторы каналов Са++ |
(нет) |
Бепридил |
(нет) |
(нет) |
Бепридил |
|
Сердечные |
(нет) |
Амиодарон Флекаинид Пропафенон Квинидин |
(нет) |
(нет) |
(нет) |
|
Препараты, снижающие концентрацию липидов |
Симвастатин Ловастатин |
Симвастатин Ловастатин |
Симвастатин Ловастатин |
Симвастатин Ловастатин |
Симвастатин Ловастатин |
|
Антимикобактериальные |
Рифампин |
(нет) |
Рифампин Рифабутин |
Рифампин |
Рифампин |
|
Антигистаминные |
Астемизол Терфенадин |
Астемизол Терфенадин |
Астемизол Терфенадин |
Астемизол Терфенадин |
Астемизол Терфенадин |
|
Препараты для ЖКТ |
Цизаприд |
Цизаприд |
Цизаприд |
Цизаприд |
Цизаприд |
|
Нейролептик и |
(нет) |
Клозапин Пимозид |
(нет) |
(нет) |
(нет) |
|
Психотропные |
Мидазолам Триазолам |
Мидазолам Триазолам |
Мидазолам Триазолам |
Мидазолам Триазолам |
Мидазолам Триазолам |
|
Эрготалкалоиды (вазоконстрикторы) |
Дигидроэрготамин Эрготамин ** (различные формы) |
Дигидроэрготамин Эрготамин ** (различные формы) |
Дигидроэрготамин Эрготамин ** (различные формы) |
Дигидроэрготамин Эрготамин ** (различные формы) |
Дигидроэрготамин Эрготамин ** (различные формы) |
* Некоторые из перечисленных препаратов включены в таблицу по теоретическим соображениям. Например, в таблицу включены лекарства, которые могут вмешиваться в метаболизм цитохрома Р450 или в другие пути метаболизма. У конкретных больных лекарственные взаимодействия могут иметь место, но могут и отсутствовать.
** Это, вероятно, эффект, присущий для всего класса лекарств.
Продолжение таблицы
|
Группа лекарств |
Невирапин |
Делавирдин |
Ифавиренц |
|
Блокаторы каналов Са++ |
(нет) |
(нет) |
(нет) |
|
Сердечные |
(нет) |
(нет) |
(нет) |
|
Препараты, снижающие концентрацию липидов |
(нет) |
Симвастатин Ловастатин |
(нет) |
|
Антимикобактериальные |
(нет) |
Рифампин Рифабутин |
(нет) |
|
Антигистаминные |
(нет) |
Астемизол Терфенадин |
Астемизол Терфенадин |
|
Препараты для ЖКТ |
(нет) |
Цизаприд Блокаторы Н-2 Ингибиторы протонной помпы |
Цизаприд |
|
Нейролептики |
(нет) |
(нет) |
(нет) |
|
Психотропные |
(нет) |
Мидазолам Триазолам |
Мидазолам Триазолам |
|
Эргот-алкалоиды (вазокон-стрикторы) |
(нет) |
Дигидроэрготамин (Д.Г.Э. 45) Эрготамин ** (различные формы) |
Дигидроэрготамин (Д.Г.Э. 45) Эрготамин ** (различные формы) |
** Это, вероятно, эффект, присущий для всего класса лекарств.
Исследованиями, проведенными сотрудниками Института тропической медицины и гигиены в Антверпене (проанализировали результаты применения современных схем комбинированной терапии более чем у 1000 больных из нескольких стран Европы) установлено, что регулярный прием ингибиторов протеазы отрицательно влияет на сексуальную активность пациентов. Снижение либидо отметили почти половина (48 %) мужчин и треть женщин, получавших высоко активную антиретровирусную терапию с использованием в схеме ингибиторов протеазы, а у 44 % мужчин, принимавших эти препараты, наблюдалось снижение потенции (при лечении другими ингибиторами вируса иммунодефицита - только у 27 % мужчин
Накопленный за эти годы опыт показал, что принцип подхода к лечению больных ВИЧ-инфекцией – как при диабете - пожизненное применение антиретровирусных препаратов. Правда в последнее время разрабатывается схема прерывистого приема лекарственных средств с тенденцией все возрастающих «окон» между циклами приема.
К сожалению, даже при положительном эффекте не прекращается репликация вируса. Эффект от терапии сравнительно не продолжителен. При самом оптимальном варианте больной должен настроиться на лечение в течение 20-30 лет.
Сегодня помимо проблемы оптимальной комбинации препаратов стоят на повестке дня многие другие вопросы: а) когда начинать лечение ретровирусной инфекции? б) комбинация каких препаратов будет наилучшей в начальной стадии? в) на чем должны основываться изменения лечебной тактики - на уровне вирусной нагрузки, количестве клеток СD4+ , обоих этих показателях одновременно или критерием является ранний регресс клинической симптоматики? г) как учитывать токсичность препаратов?
Например, установлено, что комбинация зидовудина с
диданозином и зальцитабином лучше, чем просто зидовудин в начале лечения, но не
решена проблема, какова эффективность комбинации зидовудина и ламивудина,
которая сейчас настоятельно рекомендуется, или комбинации с ингибиторами
протеаз.
Сложной остается ситуация с больными, ранее принимавшими зидовудин. Примером
могут служить результаты двух клинических испытаний AIDS Clinical Trial Group
(ACTG) 175 и Delta, проведенных в Европе и Австралии, которые продемонстрировали
преимущества комбинированной терапии у больных, никогда не получавших зидовудин.
Исследования ACTG 175 показали, что применение только диданозина или в сочетании
с зидовудином дает лучшие результаты, чем монотерапия зидовудином. Материалами
Delta установлено, что эффективность монотерапии зидовудином и комбинированного
лечения существенно не различается. По данным исследований ACTG 175 и Delta
следовало отдать предпочтение использованию комбинации зидовудина и диданозина,
а на деле монотерапия диданозином дала лучшие клинические результаты.
Однако, определение значений суррогатных маркеров, примененных в исследованиях,
не дает представления о токсичности препаратов.
Индикатором токсичности может быть количество больных-участников исследования,
продолжающих принимать изучаемый препарат. Так, из исследования ACTG 175 по
разным причинам выбыло 50% больных, в исследовании Delta из группы принимавших
зидовудин выбыло 70% пациентов из-за токсичности препарата, возможности
переключиться на альтернативное лечение или получать препараты из клубов
покупателей. Как справедливо отмечает
M. S. Hirsch (1998), проводить подобные исследования и получать конечные
результаты будет все труднее и труднее. Видимо, придется в будущих исследованиях
ориентироваться на суррогатные маркеры, и похоже, что вскоре определение
количества копий вирусной РНК в крови больных станет такой же обычной
процедурой, как и измерение артериального давления у больных гипертонией или
определение уровня глюкозы у пациентов с диабетом.
Интерферон. В группу лекарственных средств с
противовирусной эффективностью с одновременным иммуномодулирующим эффектом в
настоящее время широкое распространение получили препараты интерферона и
индукторы эндогенного интерферона. При лечении интерфероном к наиболее частым
побочным проявлениям относится так называемый гриппоподобный синдром, который
развивается через 3-5 ч после введения препарата и характеризуется повышением
температуры, миалгиями, артралгиями, головной болью. Довольно тяжело этот
синдром протекает после первой инъекции и обычно значительно уменьшается в
течение 1-й и 2-й недель лечения. Степень выраженности синдрома можно
значительно уменьшить при применении интерферона перед сном и назначении
парацетамола и/или нестероидных противовоспалительных препаратов во время
введения интерферона и на следующее утро.
Частым осложнением интерферонотерапии является снижение тромбоцитов и
лейкоцитов, которое наиболее выражено у больных циррозом печени и развивается
обычно на 2-4-м месяце лечения. Редкими побочными проявлениями являются снижение
аппетита и потеря массы тела во время лечения, которые не требуют отмены
лечения. Иногда побочная реакция проявляется в виде депрессии, которая чаще
развивается у больных, имеющих отягощенный психический анамнез.
Нестероидные противовоспалительные препараты с выраженным противовоспалительным эффектом представлены группой пиразолидонов, производных индолуксусной кислоты, производных фенилуксусной кислоты, оксикамы, производных пропионовой кислоты. В группу препаратов со слабой противовоспалительной активностью входят производные антраниловой кислоты, пиразолоны (в том числе анальгин, амидопирин), производные парааминофенола (фенацетин, парацетамол) и др.
В среднем у 0,1-0,5 % населения встречается непереносимость анальгетиков. У больных с хронической крапивницей, астмой с поллинозом частота непереносимости этих препаратов значительно возрастает, достигая 10-18 %.
Среди побочных эффектов всех НПВС является высокий риск развития реакций со стороны желудочно-кишечного тракта. У трети больных, получающих НПВС, отмечаются диспептические расстройства, у 10-20 % - эрозии и язвы желудка, у 2-5 % - кровотечения и перфорации. именно в связи с побочными эффектами со стороны желудочно-кишечного тракта выделен специфический синдром - НПВС-гастродуоденопатия. Причем, он лишь отчасти связан с локальным повреждающим влиянием НПВС на слизистую, а, в основном, обусловлен системным действием препаратов. Поэтому гастротоксичность может иметь место при парентеральном или ректальном введении НПВС.
Индуцированное НПВС повреждение чаще отмечается у женщин, оно локализуется преимущественно в антральном и препилорическом отделе желудка, проявляясь в виде эритемы слизистой оболочки, эрозии, язвы, кровоизлияния. Существует различие между язвами, вызванными приёмом НПВС и спонтанно возникшей язвенной болезнью: вызванные приёмом НПВС язвы в 60% бывают бессимптомными, особенно у пожилых и диагностируются как случайная находка при фиброгастродуоденоскопии. Специально проведенное эндоскопическое обследование показало, что у больных, принимающих непрерывную терапию НПВС на протяжении 6 месяцев, лишь в 32 % слизистая желудка остаётся в норме, а у оставшихся (2/3 больных) выявляются патологические изменения, причем, слизистая оболочка вокруг язвы, вызванной НПВС, обычно нормальная или только слегка воспалена в отличие от хронического гастрита при типичной язвенной болезни желудка.
У отдельных больных первым проявлением НПВС-гастродуоденопатии является угрожающие жизни кровотечения из желудочно-кишечного тракта.
Ацетилсалициловая кислота (аспирин) нашла широкое применение в малых дозах для профилактики инфаркта миокарда. Исследования, проведенные британскими врачами и использовавшими данные о 66 тысячах пациентов, показало, что при длительном приеме аспирина даже в малых дозах вероятность гастроэнтерального кровотечения увеличивается почти в 2 раза - 2,5% по сравнению с 1,4% для пациентов, не принимающих аспирин. Среднее число таблеток аспирина, способных вызвать повреждение в желудке, составляет 106 в год [Hennekens C.H. et al., 1989; Hirsh J. et al., 1995].
Чрезмерное увлечение аспирином населения заставляет административные органы предпринимать ответные шаги по ограническию его потребления. Так, с наступлением ежегодного сезона гриппа врачи США предупреждают, что при гриппе не стоит принимать аспирин или другое жаропонижающее. Ибо известно, что вызываемая гриппом лихорадка является естественной защитной реакцией организма на инфекцию. Принимая жаропонижающее, человек только мешает организму самому справиться с заболеванием. А поэтому процесс борьбы с вирусом затягивается, продлевая болезнь как минимум на 3 дня. К примеру, врачи штата Мерилэнд выяснили, что больные гриппом, принимавшие аспирин, в среднем болели 8-9 дней, тогда как те же, кто не принимал жаропонижающих, поправлялись уже через 5 дней.
Ко-факторами развития НПВС-гастропатии являются возраст старше 65 лет, курение, злоупотребление алкоголем, наличие в анамнезе заболеваний желудочно-кишечного тракта, сопутствующий приём глюкокортикоидов, иммуносупрессантов, антикоагулянтов, длительная терапия НПВС, приём больших доз или одновременный приём двух или более препаратов этой группы.
Среди НПВС наиболее высокой ульцерогенный потенциал у таких препаратов, как пироксикам, кетопрофен и толметин, а наименьший – у ибупрофена и диклофенака. В таблицах 35 и 36 представлены сравнительный риск и индексы гастроинтестинальной токсичности НПВС (соотношение доз, вызывающих в 50% случаев противовоспалительный и ульцерогенный эффекты).
Таблица 35
Сравнительный риск возникновения эрозивно-язвенных поражений при приеме НПВС (Garcia Rodriguez L. A., 1998)
|
Препарат |
Число работ, взятых для метаанализа. |
Относительный риск (М ± m). |
|
Ибупрофен |
11 |
1,0 ± 0 |
|
Диклофенак |
8 |
2,3 ± 0,5 |
|
Дифлунизал |
2 |
3,5 ± 0,5 |
|
Фенопрофен |
2 |
3,5 ± 1,2 |
|
Аспирин |
6 |
4,8 ± 0,5 |
|
Сулиндак |
5 |
6,0 ± 0 |
|
Напроксен |
10 |
7,0 ± 0 |
|
Индометацин |
11 |
8,0 ± 0 |
|
Пироксикам |
10 |
9,0 ± 0 |
|
Кетопрофен |
7 |
10,3 ± 0,5 |
|
Толметин |
2 |
11,0 ± 0,9 |
|
Азапропазон |
2 |
11,7 ± 0,5 |
Таблица 36
Индекс гастроинтестинальной токсичности различных НПВС
|
Препарат |
Число больных |
Индекс токсичности |
|
Салсалат |
187 |
0,81 ± 0,51 |
|
Ибупрофен |
577 |
1,13 ± 0,29 |
|
Аспирин |
1521 |
1,18 ± 0,18 |
|
Сулиндак |
562 |
1,68 ± 0,29 |
|
Диклофенак |
415 |
1,81 ± 0,35 |
|
Напроксен |
1062 |
1,91 ± 0,21 |
|
Толметин |
243 |
2,02 ± 0,44 |
|
Пироксикам |
814 |
2,03 ± 0,24 |
|
Фенопрофен |
158 |
2,35 ± 0,55 |
|
Индометацин |
418 |
2,39 ± 0,34 |
|
Кетопрофен |
259 |
2,65 ± 0,43 |
|
Меклофеномат |
165 |
3,91 ± 0,54 |
В целях улучшения переносимости НПВС рекомендуется изменение тактики их применения, а именно, снижение дозы и переход на парентеральное, ректальное или местное введение. Правда, в силу того, что НПВС-гастродуоденопатия является не столько местной, сколько системной реакцией, последний подход не решает проблему полностью.
Новым словом в этом направлении является попытка создать НПВС, освобождающих оксид азота (NO), который, поддерживая гастроинтестинальный кровоток и ингибируя адгезию и активацию нейтрофилов, препятствует проявлению ульцерогенного действия НПВС. Примером этого поколения НПВС можно назвать диклофенак, обогащенный донором NO.
В связи с успехами изучения этиологии язвенной болезни в настоящее время обсуждается целесообразность проведения у Helicobacter pylori (Hp)-положительных больных, получающих НПВС, эрадикационной антигеликобактерной терапии. Согласительная конференция европейской группы по изучению Helicobacter pylori (Маастрихт, 1996) отнесла необходимость применения НПВС у Hp-положительных больных ко второй категории показаний к эрадикационной антигеликобактерной терапии ("терапия может оказаться полезной"). Проведение такого курса является особенно целесообразным у тех лиц, у которых в анамнезе имелись указания на наличие язвенной болезни, поскольку уничтожение Hp в таких случаях снижает риск её обострения на фоне применения НПВС.
Таким образом, в связи с отрицательными эффектами НПВС противопоказаны при эрозивно-язвенных поражениях желудочно-кишечного тракта, особенно в стадии обострения, выраженных нарушениях функции печени и почек, цитопениях, индивидуальной непереносимости, беременности. При необходимости наиболее безопасными являются небольшие дозы аспирина. Нельзя применять фенилбутазон и содержащие его комбинированные препараты (реопирин, пирабутол) как анальгетики или антипиретики в широкой клинической практике. С осторожностью следует назначать НПВС больным бронхиальной астмой. У лиц пожилого возраста необходимо стремиться к назначению минимальных эффективных доз и коротких курсов НПВС.
Второе место по значимости нежелательных реакций терапии НПВС занимает нефротоксичность. В основе ее лежат:
– сужение сосудов и ухудшение почечного кровотока путём блокады синтеза ПГ-Е2 и простациклинов в почках, что ведёт к развитию ишемических изменений в почках, снижению клубочковой фильтрации и объёма диуреза с нарушением водно-электролитного обмена (особенно при приеме индометацина и фенилбутазона, бутадиона);
– прямое воздействие на паренхиму почек, вызывая интерстициальный нефрит – "анальгетическая нефропатия" (чаще при приеме фенацетина, бутадиона, анальгина, индометацина, ибупрофена).
Лекарственная нефротоксичность чаще развивается у лиц старше 65 лет, к ее развитию также предрасполагают заболевания печени, предшествующая почечная патология, снижение объёма циркулирующей крови, гипонатриемия, длительный приём НВПС, сопутствующий приём диуретиков, сердечная недостаточность, артериальная гипертензия, избыточная масса тела, алкоголизм, состояние после оперативных вмешательств.
К осложнениям терапии НПВС также относятся гематологические изменения в виде гипохромной микроцитарной анемии, гемолитической анемии, тромбоцитопении (последние две формы имеют иммуноаллергическую природу). Чаще эти осложнения развиваются на фоне приёма производных пиразолона, индометацина, ацетилсалициловой кислоты (в лечебной практике применяется 170 препаратов, содержащих ацетилсалициловую кислоту). В большинстве случаев отмена препарата приводит к нормализации гемограммы в течение 1-2 недель. Но возможно тяжелое течение осложнения, связанное со стойким угнетением кроветворения в костном мозге, которое клинически проявляются лейкопенией, агранулоцитозом, тромбоцитопенией. Обычно они развиваются при приеме анальгина и фенацетина.
НПВС могут обусловить и гепатотоксическое действие, развивающееся по иммуноаллергическому, токсическому или смешанному механизму. Так, производные пиразолона могут обусловить иммуноаллергический гепатит уже в начале их приема. При приеме в течение нескольких месяцев фенилбутазона, сулиндака и диклофенака натрия может развиться токсический гепатит с клиникой желтухи.
Так как НПВС хорошо проникают через гемато-энцефалический барьер (в 1-6 %, а при использовании индометацина - до 10 % случаев, возможно побочное действие их на нервную систему , которое проявляется головокружением, головными болями, чувством утомления и расстройствами сна. При приеме индометацина возможно развитие ретинопатии и кератопатии за счет отложения препарата в сетчатке и роговице, а длительный прием ибупрофена может привести к развитию неврита зрительного нерва. В 1,5-4 % случаев наблюдаются нарушения психики в виде галлюцинаций, спутанности сознания при приеме индометацина, что обусловлено высокой степенью проникновения препарата в ЦНС.
Аллергические реакции на прием НПВС со стороны кожи и слизистых оболочек составляют 12-15 % всех побочных реакций. Они чаще отмечаются при использовании пиразолонов и пиразолидинов и имеют весьма многообразные проявления от доброкачественного течения зудящей скарлатино- и кореподобной сыпи, фотосенсибилизации или крапивницы, сопровождающейся отёком до тяжелых проявлений в виде полиморфной эритемы (на любой препарат), пигментной фиксированной эритемы (специфичной для препаратов пиразолонового ряда), синдрома Стивенса-Джонсона, Лайелла.
Повышенная чувствительность на ацетилсалициловую кислоту выявляется у 0,3 % населения, приблизительно у 20 % больных с хронической крапивницей, у 5-20 % больных бронхиальной астмой и у 30-40 % больных бронхиальной астмой и носовыми полипами. Повышенная чувствительность к ней встречается с большей частотой у людей 30-60 лет, чем у детей; у женщин чаще, чем у мужчин. Ацетилсалициловая кислота может явиться причиной аллергического ринита, конъюнктивита, синдрома Видаля (сочетание ринита, поллиноза слизистой носа, бронхиальной астмы и крапивницы), гиперэозинофилии, а в 0,01-0,5 % всех осложнений составляют тяжелые осложнения в виде анафилактического шока и отёка Квинке.
В группе лекарственных средств, способных индуцировать тяжелые обострения бронхиальной астмы первое место занимают ацетилсалициловая кислота и анальгетики. Больным бронхиальной астмой, имеющим такие проявления, как отек слизистой носа, полипозные разрастания, периорбитальный отек, уртикарные высыпания, необходимо с настороженностью подходить к назначению нестероидных противовоспалительных препаратов. Среди больных так называемой аспириновой астмой самый высокий процент смертельных исходов, что связывают с неосторожным назначением врачами НПВС. Больным этой формой заболевания предпочтительнее назначение системных стероидных препаратов. В последние годы стали назначать ингибиторы лейкотриеновых рецепторов, что значительно улучшило прогноз при непереносимости аспирина [Чучалин А.Г. ,2000].
Для некоторых НПВС свойственен тератогенный эффект. Так, ацетилсалициловая кислота при приеме в первом триместре беременности в 8-14 случаев на 100 наблюдений приводит к развитию расщепления верхнего неба у плода. НПВС при приеме в последние недели беременности, особенно индометацина, обусловливают торможение родовой деятельности, индометацин может привести к преждевременному закрытию артериального протока у плода, что вызывает гиперплазию лёгочных сосудов и гипертензию в малом круге кровообращения.
Обладают НПВС также мутагенностью и канцерогенностью. Так, у 0,8 % больных, принимавших в течение 6-12 месяцев бутадион в суточной дозе более 0,45 г. описано развитие острого лейкоза. Выявлено также развитие рака мочевого пузыря под влиянием фенацетина. Поэтому во многих странах фенацетин запрещён к применению.
Все вышеперечисленные сравнительно частые и серьезные осложнения привели к запрету на применение в ряде стран флуфенамовой кислоты, индопрофена, беноксапрофена, зомакса, оксифенбутазона, изоксикама. Из медицинского применения исключен амидопирин ввиду возможной канцерогенности. В то же время у нас в аптечную сеть продолжают поступать препараты, содержащие амидопирин, например, реопирин и многие другие.
На основании тридцатилетнего изучения D. Moneret-Vautrin (1977) выделены факторы, способствующие развитию анафилактоидных реакций при общей анестезии. К этим факторам относятся: 1) наличие атопических заболеваний, при которых выявляется повышенная готовность к высвобождению гистамина и образование IgE; 2) наличие медикаментозной аллергии в анамнезе; 3) гиперреактивность на гистамин; 4) наличие латентной спазмофилии; 5) характер анестезирующих веществ, тип анестезии и метод введения препаратов в организм (при введении анестезирующих веществ виутривенно риск увеличивается в 10 раз); 6) возможность влияния нескольких перечисленных факторов. По данным литературы, применение общей анестезии у лиц, не страдающих аллергическими заболеваниями, вызывает анафилактоидные реакции в 3,7 %, у лиц с медикаментозной аллергией в анамнезе – в 16 %.
По данным Н. Vignon (1977), анафилактоидные реакции при применении анестетиков возникают через несколько секунд или минут после введения шокогенного препарата и не зависят от стадии операции. Клинически они чаще характеризуются сочетанием бронхоспазма и кожных реакций, кожной реакции и кардиоваскулярного коллапса. Чаще реакции отмечаются у лиц, перенесших подобные реакции при прошлых оперативных вмешательствах.
Анализ данных литературы свидетельствует, что наблюдающийся при общей анестезии шок носит все признаки анафилаксии. У этих больных остро развивается биологическая смерть, имеет место всегда кардиоваскулярный коллапс, тахикардия или брадикардия, поражение кожи и органов дыхания по типу ларинго- бронхоспазма, отека Квинке, а также быстрый регресс осложнения после применения соответствующей терапии. Патогенез анафилактического шока при применении анестетиков не изучен, одни его связывают с приобретенной аллергией, другие — с гистаминвысвобождающимся эффектом.
По статистическим данным в популяции населения в 1-3 % формируется повышенная чувствительность на барбитураты после их приема. Чаще носят аллергический характер и проявляются в виде уртикарой, многоформной и скарлатиноподобной сыпи, разнообразных эритем, синдрома Стивена-Джонсона. Этот тип ГЗТ чаще возникает у лиц с такими аллергическими заболеваниями, как астма, ангионевротический отек. Протекают осложнения лечения барбитуратами обычно доброкачественно и после отмены препарата проходят. Но при приеме дифенина, чаще используемого и как противосудорожный препарат и антиаритмик, возможно развитие экзантемы или в виде синдрома, напоминающего сывороточную болезнь или инфекционный мононуклеоз. У больных через 1-6 недель от начала лечения развиваются высыпания и повышается температура тела, после чего наблюдается увеличение лимфатических желез и развивается гепатит, значительно реже - нефрит и гемолитическая анемия.
Сердечно-сосудистые препараты являются причиной осложнений у 2-8 % больных [Ridker P.M., 1998]. Побочные реакции в большинстве своем развиваются в результате высокой токсичности сердечных гликозидов или антиаритмических средств, токсическое действие которых проявляется при передозировке препарата или их кумуляции в организме больного. Токсичность препаратов проявляется даже при терапевтических дозах у лиц с поражением почек и гепато-билиарной системы.
По данным В. Г. Кукеса (1973), при лечении сердечными гликозидами побочные реакции чаще развиваются в случаях использования лантозида (34,2%), а строфантин, изоланид, ацедоксин, дигоксин обусловливают интоксикацию у 26-29 % леченых. Причем прогрессирование сердечной недостаточности ведет к увеличению интоксикации гликозидами с 12 до 46 %. Клинически интоксикация проявляется сердечно-сосудистыми (92 %), диспептическими (37 %) и нервнопсихическими нарушениями (8,4 %). Среди сердечно-сосудистых расстройств чаще всего отмечаются экстрасистолия предсердий (12%) и желудочков (73 %). У 11,6 % больных развилась пароксизмальная суправентрикулярная тахикардия, у 15,5 % — нарушение проводимости. Характерным для интоксикации гликозидами является падение суточного диуреза.
Обладая высоким раздражающим эффектом, сердечные гликозиды при их применении вызывают нарушение функции желудочно-кишечного тракта. Появляется потеря аппетита до развития анорексии, тошнота, рвота, диарея, боли в животе, гастралгия. По данным R. Fowler и сотр. (1970), при назначении детям сердечных гликозидов рвота возникает у 93% больных. Гликозиды вызывают нарушение сна у 81 % больных, а при длительном применении препаратов наперстянки возможно развитие психозов или психических расстройств. Иногда эти препараты вызывают расстройство цветного зрения, а в тяжелых случаях – ретробульбарные параличи, поражение зрительного нерва, нарушение слуха, развитие невралгий тройничного, седалищного, локтевого нервов, люмбалгий.
Сердечные гликозиды оказывают токсическое действие на функцию почек - возможно развитие почечной недостаточности.
Наиболее частые нарушения при передозирозке сердечных гликозидов развиваются со стороны сердечно-сосудистой системы. Так, препараты наперстянки у 10 % больных вызывают чувство давящей боли в области сердца.
Под влиянием сердечных гликозидов нарушается электролитный обмен, к которому чувствительна в первую очередь сердечная мышца, причем развитие гипокалиемии и гиперкальциемии является основным моментом в возникновении расстройства сердечного ритма. Нарушения сердечного ритма проявляются в виде брадикардии, экстрасистолии, тахикардии синусовой, пароксизмальной, предсердной, желудочковой. Грозным осложнением дигиталисной терапии является фибрилляция желудочков, приводящая к летальному исходу. При лечении сердечными гликозидами у 3/4 больных развивается брадикардия, более чем у половины — атриовентрикулярная блокада. Очень часто у детей регистрируется выпадение пульса (87 %).
Аллергические осложнения, вызываемые сердечными гликозидами, развиваются крайне редко и носят легкий характер. Возможно появление кожной сыпи — эритематозной, папулезной, уртикарной, развитие крапивницы и отека Квинке, зуда. У лиц с повышенной чувствительностью иногда развивается озноб, бледность кожи, похолодание конечностей.
Осложнения, вызываемые антиаритмическими средствами, могут иметь тяжелую клиническую картину. Чаще всего при передозировке препаратов или быстром внутривенном введении их развиваются опасные для жизни состояния: падение артериального давления вплоть до развития коллапса, потеря сознания, угнетение дыхания и его остановка, нарушение сердечного ритма и остановка сердца, развитие бронхоспазма, судорог по типу эпилептиформного припадка. У 1/4 больных при внутривенном и пероральном применении новокаинамида наблюдается уширение комплекса QRS, кроме того, иногда он вызывает блокаду пучка Гиса.
По данным Г. Маждракова и П. Попхристова (1976), внутривенное введение антиаритмических средств в четверти случаев вызывает уширение комплекса QRS, а умеренные дозы хинидина у 10-12 % больных стимулируют уширение данного комплекса на 50 %.
При приеме антиаритмических средств выявляются нарушения нервно-психической функции. Появляется головная боль, головокружение, психомоторное возбуждение, бессонница, галлюцинации, депрессивные состояния, затемнение сознания, бред. Одновременно могут развиваться нарушения зрения и слуха, вплоть до полной их потери.
Аллергические поражения характеризуются появлением сыпи, зуда, подъемом температуры, развитием ангионевротического отека или крапивницы, возможно развитие системной красной волчанки при длительном или повторном применении препаратов, описано развитие пурпуры от приема хинидина.
Осложнения, развивающиеся в ответ на введение коронаролитиков, чаще всего имеют аллергический, реже – токсический характер. Кожные поражения проявляются в виде зуда, сыпи, покраснения или бледности кожи, крапивницы, отека слизистых. Возможно развитие одышки, приступов удушья, бронхоспазма, отека Квинке.
Прием коронаролитиков вызывает иногда боли в области сердца, переходящие в стенокардию.
Спазмолитические средства стимулируют иногда повышение внутричерепного и внутриглазного давления, вызывая при этом расстройство зрения. Описаны анафилактоидные реакции, развившиеся от приема дибазола и компламина [Белозеров Е.С., 1989].
Нервно-психические расстройства характеризуются появлением головокружения, головной боли, бессонницы, раздражительности. Поражения со стороны крови характеризуются развитием переходящей метгемоглобинемии, устраняющейся при отмене препарата.
Появившиеся в клинической практике после 1958 г. бета-адреноблокаторы анаприлин и др. нашли широкое применение в клинической практике как антиаритмические средства. Их способность специфически блокировать эффекты связана с действием симпатических нервных импульсов [Машковский М.Д., 1998]. Однако накопленный клинический опыт показал, что препараты этой группы нередко ведут к тяжелым осложнениям. Н. Lydtin (1977) выделяет 3 группы побочных реакций бета-адреноблокаторов: прямое фармакологическое действие; вторичное действие и осложнения, связанные с индивидуальной повышенной чувствительностью к препаратам. К прямым побочным реакциям относятся усиление сердечной недостаточности, тяжелая брадикардия и гипотония, абдоминальные болевые кризы, а также тошнота и понос. Замедление сердцебиения и снижение ударного объема ведут к декомпенсации сердечной деятельности. У больных с синусовым ритмом под влиянием бета-адреноблокаторов может развиться тяжелая брадикардия и атриовентрикулярная блокада. Усиление бронхоконстрикции у больных бронхитом и особенно у больных бронхиальной астмой прием препаратов может повлечь за собой приступ астмы.
Н. Lydtin (1977) наблюдал у 25 из 268 стационарных вольных, леченных бета-адреноблокаторами, побочные реакции, в том числе у 8 – в виде отека легких, полной блокады или стенокардии. В других исследованиях из 1500 наблюдаемых больных у 6,28 % развились летальные осложнения от употребления препаратов и у 15 % осложнения, связанные с их отменой.
Помимо абдоминальных болевых кризов такой бета-адреноблокатор, как практолол вызывает перитонит, что впервые было отмечено в 1974 г. A. Marshall и соавт. (1977) описывают личные наблюдения перитонита, возникшего у 16 больных в результате приема практолола в дозе 200-400 мг/день. В большинстве случаев больные получали бета-адреноблокатор длительное время (2 года и более). До клиники перитонита у больных часто проявлялись такие медикаментозные реакции, как поражение кожи и глаз в виде сухости, изъязвление роговицы, часто в сочетании с кожными высыпаниями (у 8 из 9 человек).
Бета-блокаторы и ингибиторы ангиотензинпревращающего фермента (иАПФ) относятся к числу бронхоконстрикторов, поэтому они противопоказаны больным бронхиальной астмой. В клинической практике встречаются больные ишемической болезнью сердца, которые длительное время успешно лечатся этой группой препаратов, однако часто после перенесенного вирусного заболевания их прием начинает провоцировать бронхоспазм. Другая распространенная группа препаратов, назначаемая у больных кардиологического профиля – иАПФ. Они в достаточно высоком проценте случаев (более чем в 30%) приводят к кашлю и более чем в 4% вызывают обострение бронхиальной астмы. Необходимо отметить, что ингибиторы рецепторов ангиотензина не провоцируют возникновение кашля и обострения бронхиальной астмы [Чучалин А.Г., 2000].
За рубежом при лечении коронарной недостаточности применялся пергексилин (пексид), уменьшающий частоту приступов стенокардии у 68,7% и снижающий потребление нитроглицерина у 78,7 % больных [Dalla, Volta, 1976]. Однако накопленный клинический опыт показал, что пергексилин при длительном применении вызывает поражения периферической нервной системы.
В связи с тем, что глюкокортикоиды являются природными гормонами или их синтетическими аналогами, они не имеют абсолютных противопоказаний к назначению, а в неотложных случаях гормоны применяются вообще без учета противопоказаний. Относительными же противопоказаниями являются: язвенная болезнь желудка и двенадцатиперстной кишки в стадии обострения; (тяжелая) артериальная гипертензия; туберкулез (кроме туберкулезного перикардита); острые вирусные инфекции (герпес, ветряная оспа и др.); период вакцинации; беременность; тяжелая почечная и сердечная недостаточность; склонность к тромбоэмболическим осложнениям; выраженный остеопороз; болезнь и синдром Иценко – Кушинга; сахарный диабет (наиболее опасны фторированные глюкокортикоиды); психозы, эпилепсия.
Среди глюкокортикостероидов преднизолон рассматривается как стандартный препарат для фармакодинамической терапии. Соотношение глюкокортикоидной и минералокортикоидной активности преднизолона составляет 300:1. Метилпреднизолон по сравнению с преднизолоном обладает несколько большей глюкокортикоидной активностью (на 20 %) и оказывает слабое минералокортикоидное действие. Триамцинолон лишен минералокортикоидной активности, поэтому у него меньшая сравнительно с другими препаратами способность задерживать натрий и воду. По сравнению с преднизолоном оказывает более выраженное (на 20 %) и длительное глюкокортикоидное действие. Но он чаще вызывает нежелательные реакции со стороны мышечной ткани («триамцинолоновая» миопатия) и кожи, в связи с чем длительное применение нежелательно. Дексаметазон по глюкокортикоидной активности в 7 раз превосходит преднизолон, он является фторированным глюкокортикоидом и не обладает минералокортикоидным действием. По сравнению с другими препаратами в большей степени подавляет функцию коры надпочечников, в связи с чем длительное применение не рекомендуется из-за опасности серьезных побочных эффектов, а именно, угнетения гипоталамо – гипофизарно – надпочечниковой оси, нарушения обменных процессов, психостимулирующего действия).
Так как в утренние часы гипоталамо-гипофизарно-надпочечниковая ось наименее чувствительна к угнетающим влияниям экзогенных кортикостероидов, в большинстве случаев гормоны назначают в виде одной утренней дозы (прежде всего препараты длительного действия), либо 2/3 - 3/4 суточной дозы принимаются утром, а оставшаяся часть – около полудня. Такая схема применения позволяет уменьшить опасность угнетения гипоталамо-гипофизарно-надпочечниковой оси и снизить риск развития остеопороза.
Различные осложнения, развивающиеся от препаратов, влияющих на процессы тканевого обмена наблюдаются в 18-39 %. Наибольшее число осложнений развивается от гормональных препаратов, удельная масса которых в общем ряду лекарственных реакций составляет 5,4 % [Лопатин А.С. и Станковская И.М., 1975] и 20-100 % побочных реакций в своей группе [Егорова и соавт., 1978].
Несмотря на значительный терапевтический эффект при назначении глюкокортикоидов, побочные реакции развиваются у половины больных [Белозеров Е.С., 1989, 1995], причем у половины из них осложнения носят выраженный характер. Э. Ф. Козловская (1974) наблюдала побочные явления различной степени тяжести у 30 % гематологически больных, получавших кортикостероидные препараты, тяжелые осложнения развились у 23,7 % из их числа, а общая летальность осложнений глюкокортикоидной терапии составила 2,7 %.
При лечении глюкокортикостероидами больных вирусным гепатитом Л. Д. Левина (1963) выявила побочные реакции у 11%, а по данным М. Е. Семендяевой и Н. В. Богдановой (1963), осложнения развились у 54% больных вирусным гепатитом и механической желтухой.
Мы [Белозеров Е.С., 1989] проследили частоту и характер осложнений кортикостероидной терапии у 621 больного вирусным гепатитом за 10 лет (табл.37 ). Все больные наряду со стероидными гормонами получали дезинтоксикационную терапию: внутривенное введение 5 % раствора глюкозы, гемодеза, полиглюкина, реополиглюкина, раствор Рингера или физиологический раствор в среднем около 1 л в сутки. Наряду с этим вводились сердечно-сосудистые препараты, витамины, в конце лечения подключали желчегонные препараты. Как правило, лечение кортикостероидными гормонами сочеталось с антибиотикотерапией. Так как гормонами в основном лечили больных с тяжелым течением вирусного гепатита, то наряду с медикаментозной терапией применяли промывание желудка и кишечника, назначали кислородную терапию, вводили кокарбоксилазу; 8,7 % больных, кроме того, получали аминокапроновую кислоту, 12,3% – 1 % раствор глютаминовой кислоты. Из общего числа леченных кортикостероидными препаратами 509 получали преднизолон, 68 – дексаметазон, остальные 44 – триамцинолом. У 593 больных лечение указанными средствами сочеталось с введением гидрокортизона, у 16 – с введением АКТГ.
Из 621 больного, получавшего стероидные гормоны, побочные реакции и осложнения выявлены у 417 человек (67,3 %), в том числе тяжелые осложнения терапии в виде желудочно-кишечного кровотечения, анафилактического шока, стероидного диабета и агранулоцитоза – у 18 больных (2,89 %). У большей части больных одновременно имелось несколько проявлений побочных реакций медикаментозной терапии. В группу осложнений и побочных реакций нами включались лишь достоверно установленные и, вероятно, связанные с гормонами реакции. Например, анафилактический шок развился у больной 21 года через несколько секунд после введения гидрокортизона, причем какой-либо контакт с антибиотиками в этот период был исключен, связать осложнение с другими лекарственными препаратами также не удалюсь.
Среди больных, давших побочные реакции и осложнения, лишь 18,9 % имели в анамнезе указание на непереносимость каких-либо лекарственных препаратов или страдали какими-либо аллергическими заболеваниями.
Таблица 37
Частота побочных реакций и осложнений кортикостероидной терапии больных вирусным гепатитом
|
Вид побочных реакций |
Частота, % |
|
Желудочно-кишечное кровотечение |
0,64 |
|
Анафилактический шок |
О,16 |
|
Агранулоцитоз |
0,64 |
|
Стероидный диабет |
1,44 |
|
Стероидная язва |
4,67 |
|
Обострение язвенной болезни |
5,798 |
|
Обострение болезни после отмены гормонов |
18,9 |
|
Кушингоид |
27,0 |
|
Психоз |
0,32 |
|
Акнеподобные высыпания |
50,0 |
|
Стрии на коже |
15,1 |
|
Обострение «дремлющей» инфекции |
5,25 |
|
Повышение артериального давления |
31,0 |
До 94 % всех побочных реакций, вызываемых глюкокортикоидными препаратами, падает на долю преднизолона [Лопатин А.С. и соавт., 1978]. Наиболее часто (до 30 %) из всех побочных проявлений гормонотерапии развивается кушингоид [Егорова Л.И. и соавт., 1978]. Нередким осложнением гормонотерапии является диабет, хотя сведения о его частоте разноречивы. Так, развитие стероидного диабета регистрируется в 0,2 % случаев в наблюдениях Я. Б. Максимович (1979), а по данным В. А. Выдрина (1962) – в 80%.
Гормоны вызывают нарушения жирового обмена примерно у четверти больных, а также оказывают влияние на функциональное состояние коры надпочечников каждого шестого. Глюкокортикостероидная терапия зачастую осложняется острым или хроническим синдромом отмены, т. е. развитием острой или хронической недостаточности коры надпочечников, так как в результате длительного применения гормонов происходит снижение функции коры надпочечников или их атрофия.
Общее нарушение функции желудочно-кишечного тракта гормоны вызывают в 24,4 % случаев, а ульцерогенное действие препаратов, особенно при их пероральном применении, проявляется в 3,5-7,5 %. По данным Л. И. Егоровой и соавт. (1978), ульцерогенное действие стероидов проявлялось клинически с рентгенологическим подтверждением у 0,53 % больных, а паталогоанатомически выявлялось в 1,04% случаях.
По данным разных автором, нервно-психические нарушения от глюкокортикоидов развиваются примерно у 4-36 % больных и носят нестойкий, легкий характер в виде нарушения настроения, сна, повышенного возбуждения, чувства тревоги, головной боли.
Нередко при лечении кортикостероидными препаратами и АКТГ поражаются кожа и мышцы. Кожные реакции характеризуются акнеподобными высыпаниями, атрофией кожи, разрывом подкожно-жировой клетчатки, развитием склероподобных изменений и рубцов кожи. Чаще всего поражаются мышцы ног, развивается слабость, утомляемость, клинически выявляется гипотрофия или атрофия мышц нижних конечностей. Такие миопатии трудно поддаются лечению.
У детей глюкокортикоиды вызывают задержку роста ткани, резко снижая выработку гормона роста и вызывая усиленное выведение ионов кальция из организма. Нарушения усиливаются с увеличением дозы гормона и длительности его приема. По данным М. Presse (1976), рост замедлялся у 33 % детей, леченных кортикостероидными препаратами.
Офтальмологические осложнения под влиянием стероидных гормонов проявляются как у взрослых, так и у детей. Причем у детей данные осложнения регистрируются в 28,5-44,4 % случаев (Лаврецкий И.Г., 1977). Под влиянием глюкокортикоидов развивается катаракта — в результате повышенной проницаемости оболочки хрусталика, повышается внутриглазное давление, что может повлечь атрофию зрительных нервов и в результате — полную или частичную слепоту. Изменения в хрусталике обычно необратимы; внутриглазное давление восстанавливается и поражения зрительных нервов исчезают после отмены глюкокортикоидов [Kass М.А. et. аl., 1972; Hubner F. K., 1976]. Повышение внутриглазного давления у взрослых выявлено в 6,1% случаев
Несмотря на выраженное антигистаминное и десенсибилизирующее действие, глюкокортикостероидные гормоны иногда вызывают аллергические реакции. Нами отмечено развитие анафилактического шока на гидрокортизон, в литературе описаны случаи шока на кортизон, анафилактоидные реакции на преднизолон и АКТГ.
Вопрос о тератогенном действии стероидных гормонов окончательно не решен, однако накоплено достаточно данных о развитии аномалий плода и новорожденных детей при приеме во время беременности глюкокортикоидных гормонов. Чаще всего обнаруживаются мегалоглоссия, расщелина твердого нёба, размягчение костей свода черепа, стеноз аорты, умственная отсталость, детские церебральные параличи, недостаточность надпочечников, мертворожденность.
Тератогенное действие кортикостероидов изучено в эксперименте и клинике. Имеются сообщения об их канцерогенности. Синтетические нестероидные эстрогены (диэтилстильбестрол, в частности), по сообщениям зарубежных авторов, обладают неонатальным канцерогенезом у плода женского пола. Наибольшая частота развития аденокарцином влагалища и шейки матки выявляется у девушек в постпубертатном периоде, доброкачественные опухоли влагалища регистрируются у 30-40 % девушек, матери которых лечились нестероидными эстрогенными гормонами [Henry-Suchet J., Brux J., 1975]. Помимо этого, половые гормоны при введении их беременным женщинам вызывают у плода женского пола маскулиноподобный эффект.
Выраженным канцерогенным действием обладают оральные контрацептивы. Под влиянием эстрогенных оральных контрацептивов развиваются рак шейки матки, доброкачественные опухоли грудных желез, усиливается рост имеющихся в организме неоплазматических клеток. По данным Шведского комитета нежелательных лекарственных реакций, за 5 лет оральные контрацептивы явились причиной подобных осложнений в 25 % случаев.
Природные и нефторированные глюкокортикоиды при беременности в целом безопасны для плода, но при длительном приеме фторированных препаратов возможно развитие нежелательных эффектов у плода, в том числе уродств. При кормлении грудью низкие дозы гормонов, эквивалентные 5 мг преднизолона, не представляют опасности для ребенка, однако более высокие дозы препаратов могут вызвать задержку роста и угнетение гипоталамо-гипофизарно-надпочечниковой оси у ребенка. Поэтому женщинам, принимающим умеренные и высокие дозы глюкокортикоидов, не рекомендуют кормить ребенка грудью.
Витамины составляют большую группу средств, влияющих на тканевой обмен. Они активно участвуют в иммунобиологических процессах в организме, повышая его защитные силы, участвуют в качестве катализаторов в ферментативных процессах обмена жиров, белков, углеводов и минеральных элементов, обеспечивают трансформацию энергии. Основная часть витаминов поступает в организм извне – с продуктами питания, другая часть синтезируется внутри него.
Поступая в организм, витамины могут оказать как токсическое, так и аллергическое действие, частота побочных осложнений достигает 5,2 % случаев [Лопатин, 1975]. Токсическое действие развивается при избыточном поступлении витаминов в организм, что клинически проявляется в развитии гипервитаминозов. Наиболее тяжелую клинику токсических осложнений вызывают жирорастворимые витамины А, Д, Е, К.
Побочные реакции, вызываемые витамином А (ретинолом) чаще всего носят характер острого или хронического гипервитаминоза, причем, при избыточном употреблении каротина (провитамина А) отравление не наблюдается. При гипервитаминозе преобладают симптомы выраженной интоксикации, сопровождающейся в отдельных случаях развитием психозов. Через несколько часов после введения витамина на коже и слизистых появляются высыпания от петехиальных до обширных кровоизлияний и возможно развитие эксфолиативного дерматита. У детей гипервитаминоз помимо симптомов интоксикации вызывает повышение температуры и внутричерепного давления. У детей первого года жизни клинически это проявляется набуханием большого родничка. У беременных женщин гипервитаминоз нарушает развитие эмбриона, формируя уродство плода.
Витамин роста (кальциферол) чаще всего вызывает развитие гипервитаминоза, характеризующегося повышенным содержанием кальция в крови; первым диагностическим признаком является обнаружение кальция в моче. Гиперкальциемия ведет к повышенному отложению кальция в эпителии канальцев и клубочков почек, стенках сосудов, в альвеолах, слизистой глаз. Развиваются остеопороз и спонтанные переломы, несмотря на избыток кальция крови, ибо отложение его идет в надкостнице, в костной ткани наблюдаются очаги обызвествления.
Аллергические осложнения, вызываемые витаминами группы В, разнообразны по форме и тяжести. Так, акнеподобные и склероподобные изменения на коже развиваются от применения тиамина, витамина B12. Развитие феномена Артюса на месте введения витамина B12 наблюдали Купчинскас и соавт. (1972), они же описывают развитие одышки от витамина B1. При лечении витамином РР наблюдается выпадение волос, изучение влияния цианкобаламина на микрофлору кишечника выявило, что большие и средние дозы препарата вызывают повышенное выделение летучих фенолов и кратковременное изменение микрофлоры кишечника.
Наиболее грозное осложнение витаминотерапии — развитие анафилактического шока. Описано его развитие при введении тиамина, никотиновой кислоты, цианкобаламина, группы витаминов B1, B6, В12 .
Аллергические реакции при повышенной чувствительности организма к витамину С могут характеризоваться различными сыпями, зудом, крапивницей, а также развитием анафилактического шока.
Седативные средства. Основными в этой группе лекарственных веществ, используемых в терапевтической практике, являются препараты брома, валерианы и лекарственные средства растительного происхождения.
Развитие побочных явлений возможно при длительном приеме бромидов. Это состояние описано под названием «бромизм» и характеризуется появлением насморка, кашля, поражения конъюнктивы, общей слабости, расстройства пищеварения, кожных сыпей. Установлено, что содержание бромидов в крови в пределах 1 мг/мл может вызвать явления хронической интоксикации, а концентрация 2-3 мг/мл – более тяжелые расстройства. центральной нервной системы. Однако прием препаратов в терапевтических дозах редко сопровождается побочными явлениями.
Нейролептические средства. Основными препаратами в этой группе лекарств, используемых в. практической деятельности, являются производные фенотиазина (аминазин, пропазин и др.), производные индола (резерпин, раунатин). Лекарственные средства фенотиазинового ряда характеризует достаточно высокий индекс сенсибилизации при непосредственном контакте с препаратом. Так, у медицинских работников достигает 60 %. Иногда достаточно только следов препарата, чтобы развилась выраженная местная аллергическая реакция, к примеру, при прикосновении в таблетке. Это послужило основанием для выпуска препаратов в форме драже.
Клинически аллергическая реакция проявляется в виде контактного аллергического дерматита, часто встречаются экзантемы, отеки Квинке, холестаз, агранулоцитоз, который может послужить причиной летального исхода.
Первым производным фенотиазина, примененным как нейролептическое средство, был аминазин. К наиболее важным осложнениям, вызываемым аминазином, относятся расстройства пищеварения, сердечно-сосудистой системы, нервно-психические и аллергические расстройства. Н. Депбеч с соавт. (1957) из 1523 больных, принимавших аминазин, выявили побочные реакции у 18,2 %. Аналогичные результаты получили И. А. Полищук и В. Н. Вашетко (1962) при обследовании 142 больных, среди которых осложнения аминазиновой терапии составили 16,3 %.
При лечении нейролептическими препаратами, особенно аминазином, возможны побочные реакции со стороны психической деятельности в виде нейролептической депрессии. Иногда под влиянием терапии нейролептиками возникает токсический делирий.
Гепатит с желтухой считается одним из частых осложнений при лечении аминазином и составляет, по данными различных авторов, от 0,2 до 4-5 % среди применявших его. Гематологические осложнения встречаются довольно редко, из них наиболее опасен агранулоцитоз, вызывающий летальные исходы. Аминазин может значительно снижать артериальное давление, что нередко приводит к кратковременной потере сознания или сосудистому коллапсу. Особенно опасно назначение аминазина больным с резко выраженными явлениями атеросклероза сосудов головного мозга и сердца, так как при этом могут наблюдаться летальные исходы в связи со снижением кровотока в сосудах.
. В последние годы широкое применение, в медицинской практике нашли диуретические препараты, многие из которых наряду с четко выраженным терапевтическим эффектом оказывают побочные действия, в том числе и опасные для жизни больного. При лечении диуретиками развиваются водно-электролитные, метаболические и токсические осложнения. В связи с увеличением диуреза препараты этой группы всегда способствуют усиленному выведению из организма натрия и хлора. Острая и хроническая гипонатриемии чаще всего развиваются у лиц, находящихся на длительном гипонатриевом режиме. Острая потеря натрия чаще всего развивается у больных с отеками на фоне сохраненной функции почек и характеризуется быстрым уменьшением отеков, похудением, тахикардией, гипотонией, адинамией, сонливостью. Для хронической потери натрия характерны астения, мышечные подергивания, тошнота и такие психические расстройства, как дезориентация, сомноленция.
У больных с декомпенсированной сердечной недостаточностью и циррозом печени назначение диуретиков может повлечь за собой развитие гипонатриемии разведения. Этот вид гипонатриемии носит в основном субклинический характер и лишь в тяжелых случаях проявляется судорогами, мышечными подергиваниями и потерей сознания.
Довольно опасным для жизни осложнением терапии диуретиками является гиперкалиемия. Хотя клинически геперкалиемия ярко не выражена, однако в силу способности к быстрому прогрессированию и трудности коррекции она приводит к остановке сердца в результате брадикардии с последующей фибрилляцией желудочков.
Метаболические осложнения развиваются при терапии всеми видами диуретиков и проявляются гиперурикемией. Способствуют этому осложнению нарушение обмена, почечная недостаточность, ожирение в сочетании с гипокалорийной диетой, гипертоническая болезнь и диабет. К метаболическим осложнениям лечения диуретиками следует отнести развитие гипергликемии, особенно у лиц, страдающих диабетом.
Токсические осложнения при терапии диуретиками включают в себя реакции со стороны крови, желудочно-кишечного тракта, кожи, половых органов. Характер токсического действия во многом определяется видом диуретика. Так, тиазидовые диуретики чаще вызывают тромбоцитопению, сульфаниламидные диуретики — агранулоцитоз, салуретики — некротический панкреатит, фуросемид, этакриновая кислота и триамтерен – гепатит. У почечных больных ототоксический эффект оказывает этакриновая кислота; гинекомастии у мужчин и нарушение менструального цикла у женщин вызывает при длительном приеме альдактон.
5.11. Цитостатики
В настоящее время все шире применяются в медицинской практике цитостатические препараты. Эти средства назначаются как при лечении больных с новообразованиями, так и с нераковыми болезнями, в частности при коллагенозе, хроническом гепатите, язвенном колите, нефрозе, при трансплантации органов и др. Побочные действия этих препаратов связаны в основном с их цитостатическим действием на все клетки и ткани, обладающие высокой пролиферативной активностью, и в частности на лимфоидную ткань. При этом развивается вторичная, т. е. приобретенная, иммунологическая недостаточность, с которой в конечном итоге связано побочное канцерогенное «действие» цитостатических препаратов. W. Hunstein и соавт. (1975) проводят аналогию между канцерогенным действием противоопухолевых цитостатиков и радиотерапией. При этом они наблюдали развитие опухолей (рак желудка, прямой кишки, яичника, желчного пузыря, грудной железы, мочевого пузыря) при лечении циклофосфамидом в дозе 7—140г. Так, при лечении цитостатиками нераковых заболеваний из 4000 больных у 3 человек авторы обнаружили рак различных органов.
Некоторые цитостатики обладают струмогенным, тератогенным действием. Многие авторы указывают на гепатотоксическое действие цитостатических препаратов и, в частности, 6-меркаптопурина, мелфалана, биоульфана, хлорбутина н др. А. И. Воробьев и соавт. (1975) описали цитостатическую болезнь, вызванную 6-меркаптопурином, циклофосфаном, миелосаном, сарколизином, цитозинорабинозидом, натуланом, мустаргеном, ТИО-ТЭФ и лейкераном. Большинство этих препаратов оказывает разрушительное действие на эпителий кишечника. При этом авторы наблюдали у большинства больных развитие энтерита, колита, эзофагита, гастрита, у 5 из 55 больных — гепатита.
При лечении цитостатическими препаратами зачастую возникают инфекционные осложнения вследствие активации банальной инфекции.
Обобщая данные 30 госпиталей США, Канады, Австралии и Европы о побочном действии рентгеноконтрастных средств для внутрисосудистого введения 112003 больным, W. Shehadi (1975) после обработки материала на ЭВМ установил несмертельные побочные реакции в 4,95 % случаев. Наименьшая частота реакций отмечена при ангиокардиографии (1,42 %), а наибольшая при внутривенной урографии (5,65%) и холангиографии (10,1 %). Тяжелые реакции отмечены в 1,58 % осложнений, причем у 11 человек со смертельным исходом, в том числе у 6 после урографии, у 2 в результате ангиокардиографии, по 1 после венографии, холангиографии, церебральной ангиографии.
Клиника медикаментозных осложнений при использовании рентгеноконтрастных веществ характеризовалась тошнотой (33,6 %), рвотой (20,5%), крапивницей (15,5%), зудящими кожными высыпаниями (12,7%), бронхоспазмом (3,19 %), отеком Квинке (2,61%), назальгией (2,30 %), циркуляторным коллапсом (0,29 %), неврологическими нарушениями (0,27 %), остановкой сердца '(0,18 %), фибрилляцией желудочков (0,16%), отеком легких (0,08 %).
Из числа больных с медикаментозными осложнениями при применении рентгеноконтрастных веществ неблагоприятный аллергологический анамнез установлен лишь у 10,2% больных.
Проведенная W. Shehadi (1975) оценка диагностической значимости внутрикожных и подкожных проб на чувствительность к рентгеноконтрастным веществам показала отсутствие их диагностической ценности. Так, из 375 больных с положительной пробои реакция на рентгеноконтрастное вещество после введения полной дозы не развилась у 76 больных, быстро прошла без лечения у 209 больных и была купирована без прекращения введения рентгеноконтрастного вещества у 87 больных, в 3 случаях имел место летальный исход.
М.Я. Вайнтруб (1999) изучены медикаментозные осложнения у больных эпилепсией. Согласно данным литературы, частота медикаментозных осложнений при эпилепсии колеблется от 7 до 25%, что делает актуальным их раннюю диагностику и своевременную коррекцию, а также меры превенции [Ю.А. Скроцкий, 1973; Д. Dam, 1988; E.H. Reynolds et al., 1981; М.Ш. Вольф, 1991; М.Я. Вайнтруб, 1995]. Эти осложнения терапии охватывают как нарушения головного мозга, так и других систем организма, что требует специального лечения [Е.Н. Reynold, 1975; D. Smidt, 1983; А.С. Лопатин, 1984].
У больных эпилепсией осложнения медикаментозной терапии делятся на следующие варианты: 1) аллергический тип; 2) токсический; 3) метаболический; 4) фармакогенетический; 5) осложнения, возникающие вследствие фармакологической несовместимости; 6) лекарственной зависимости (синдрома отмены). Наиболее часто в психиатрической клинике встречаются аллергический, токсический и метаболический типы, реже - другие. Токсические осложнения наблюдаются при передозировке, синергическом воздействии нескольких антиконвульсантов в резистентных к терапии случаях, а также у больных с органической симптоматикой. Метаболические осложнения в основном возникают в условиях антагонизма некоторых антиконвульсантов (дилантин, фенобарбитал, гексамидин) с витаминами, при длительном их приеме.
Как отмечает М.Я. Вайнтруб (1999), гематологические изменения при осложнениях необходимо у больных эпилепсией дифференцировать от гематологических отклонений, обусловленных самим эпилептическим процессом. Последние имеют транзиторный, нестойкий характер и коррелируют только с периодом пароксизмов. При тяжелых интоксикациях общее количество лейкоцитов достигает 2300-2500, а сегментоядерных нейтрофилов - 1100-1300 в 1 куб. мм крови. Нейтропения (0,5 %) выявлялась у больных через 7-14 дней после назначения антиконвульсантов и характеризовалась снижением лейкоцитов до 3500 в 1 куб. мм и эозинофилией. Она проходила спустя несколько дней после отмены препаратов, что позволило связать ее с терапией.
По данным автора, токсические осложнения I степени в виде
сонливости и вялости, заторможенности психики и двигательных актов возникали
чаще вследствие индивидуальной передозировки барбитуратов (фенобарбитала,
гексамидина, бензонала), а также при комбинированном применении последних с
бензодиапинами, бромидами, дифенином, конвулексом и другими антиэпилептическими
препаратами. Среди психопатологических расстройств встречаются астенические,
астено-апатические, астено-субдепрессивные состояния. Часто наблюдаются
вегетативные сдвиги (брадикардия, гипотония, гипотермия), нарушения кишечной
перистальтики (запоры), а также гематологические (лейкопения с тенденцией к
нейтропении и тромбоцитопении).
При симптомах органического поражения ЦНС первая стадия интоксикации переходит
во вторую с появлением таких симптомов, как помрачение сознания в виде легкой
спутанности, нарастает мозжечковая симптоматика, появляется дизартрия,
скандированная речь, олигофазия, общая брадикинезия, появляются вертикальный
нистагм, диплопия, изменяется почерк, кроме того, учащаются припадки. Этой
психоневрологической симптоматике сопутствуют стойкие гематологические
нарушения, чаще нейтропения, тромбоцитопения, что расценивается как следствие
передозировки антиконвульсантов.
В отличие от токсических осложнений метаболические развиваются в течение 1-2 месяцев, медленно нарастают и не обнаруживают зависимости от терапевтических доз противосудорожных препаратов, обладающих антифолиевым действием. Чаще появляются астенические синдромы с субдепрессией. К особенностям метаболических осложнений относится частота соматологической патологии, особенно вследствие приема дифенина: отек и гиперемия зубодесневых сосочков, их кровоточивость, гиперплазия десен. При прогрессировании медикаментозной патологии развивается вторая стадия, для которой характерно нарастание психических расстройств в виде депрессии, апатии, мнестико-интеллектуальных нарушений.
Аллергические реакции на барбитураты, дифенин, вальпроаты,
бензодиазепины в отличие от токсических и метаболических осложнений
характеризуются большим полиморфизмом. Аллергические реакции у подавляющего
большинства (90%) больных возникает через 7-11 дней после приема указанных
препаратов.
Таким образом, как отмечает М.Я. Вайнтруб (1999), клинические проявления
лекарственных осложнений у больных эпилепсией носят системный характер и находят
отражение в психопатологических и соматических нарушениях, степень выраженности
которых имеет ряд особенностей, отражающих динамику их формирования.
Фармакологические свойства разных противосудорожных препаратов накладывают свой
отпечаток на клинические проявления осложнений. Гематологические сдвиги являются
одним из ярких индикаторов лекарственных осложнений носящих системный характер.
При многолетнем приеме противоэпилептических препаратов развитию осложнений
способствуют ряд индивидуальных особенностей организма больных: абсолютная
резистентность к препаратам вследствие врожденной или приобретенной
иммунопатологии, длительное прогредиентное течение эпилепсии, степень тяжести
органического поражения мозга.
5.14. Анаболитики
В связи с появлением в стране профессионального спорта возрос интерес к анаболическим/андрогенным стероидам и другим фармацевтическим препаратам, используемым атлетами. Среди препаратов этой группы в России доступны Aндриол, Kленбутерол, Дека-дураболин, Дианабол, Дураболин, Эсиклен (Эсиклен), HCG, Лазикс, Нольвадекс, Омнадрен, Параболан, Провирон, Сустанон (Сустан), Тестостерон Энантат, Тестостерон Ципионат, Тестостерон Пропионат, Тестостерон Терамекс, Гормоны роста, Винстрол длительного действия, Винстрол.
Андриол (действующее химическое вещество: тестостеронундеканоат) - один из немногих новых стероидов, наряду с "Метилтестостероном" является единственным орально действующим препаратом тестостерона, хотя сам тестостерон при оральном приеме совершенно недейственен, так как тотчас же при всасывании из желудочно-кишечного тракта инактивиреутся в печени.
Андриол не выказывает явлений феминизации, он используется для подготовки к соревнованиям. Прим этом препарат дает возможность организму не ощущать влияния стероида на собственную репродукцию гормона, что случается лишь в случаях длительного лечения высокими дозами. Очень быстро выводится организмом, это следует учитывать при соревнованиях с допинг-контролем. Андриол не показан женщинам, т.к. андрогенные компоненты очень сильно проявляются в организме при приеме препарата.
При использовании андриола иногда возникают явления повышенного кровяного давления, скопление жидкости в организме, акне, суперсексуальности и у женщин все это приводит к явлениям маскулинизации.
Кленбутерол (действующее химическое вещество: кленбутеролгидрохлорид) - это не стероидный гормон, а 2-бета-симпатикомиметик, хотя его можно сравнить по действию со стероидами. Он способствует значительному, качественному приросту мышц, который дополняется значительным приливом силы.
Кленбутерол обладает сильным антикатаболическим действием, т.е. снижает процент разрушающегося в мышечных клетках белка и способствует увеличению мышечной клетки. Атлеты охотно применяют Кленбутерол, особенно в конце стероидного курса, чтобы попридержать возникающую катаболическую фазу и сохранить максимум силы и мышечной массы. Кроме того, Кленбутерол обладает значительным жиросжигающим воздействием. Особенно интенсивное сжигание жира происходит при комбинировании его с препаратом гормона щитовидной железы "цитомель". При одновременном приеме анаболических/андрогенных стероидов Кленбутерол вследствие вызванного им повышения температуры тела усиливает действие этих стероидов, т.к. ускоряет белковый обмен в организме. Так как Кленбутерол не является гормональным препаратом, он не имеет типичных для анаболических стероидов побочных явлений, его применяют и женщины.
Возможными побочными эффектами Кленбутерола являются чувство беспокойства, сердцебиения, легкое дрожание пальцев, головные боли, усиленная потливость, сонливость, иногда мышечные спазмы, повышенное давление и тошнота. Все эти явления временной природы и чаще всего исчезают сами собой через 8 - 10 дней несмотря на продолжение приема препарата.
Дека-дураболин (действующее химическое вещество: нандролон деканоат) относится к самым распространенным и самым используемым инъекционным стероидом. Он обусловливает накопление в мышечной клетке азот в количестве большем, чем она отдает, что ведет к положительному азотному балансу, в силу чего мышечная клетка в этой фазе аккумулирует большее количество белка, чем обычно. Это обеспечивает хороший прирост мышечной массы и силы. При этом у большинства спортсменов наблюдается заметное скопление воды в организме, которое не так сильно как при приеме инъекционных тестостеронов, но все же ведет в высоких дозировках к упругому и водянистому внешнему виду. В связи с тем, что Дека скапливает воду в соединительной ткани, то он может облегчать или полностью устранять боли в суставах, страдающие болями в плечах, локтях, коленях, могут безболезненно тренироваться при приеме Дека-дураболина.
В связи с тем, что Дека является анаболиком длительного действия, возникает опасность скопления излишнего количества воды перед соревнованиями при более высокой дозировке.
Хотя побочные явления при приеме Деки относительно малы, все же в дозировках свыше 400 мг в неделю могут возникнуть андрогеннообусловленные явления, что выражается в повышении давления крови, в замедлении процесса свертываемости крови, что может привести к частым носовым кровотечениям и кровоточащим долго незаживающим ранам, а также усиленной деятельности сальных желез и иногда к прогрессирующему акне. Молодые атлеты иногда отмечают головную боль и сексуальную суперстимуляцию. При приеме очень высоких доз в течении более продолжительного времени у мужчин могут наступить задержки сперматогенеза, т.е. яички будут продуцировать меньшее количество тестостерона. В этом причина того, что Дека-дураболин, как почти все стероиды, вызывает задержку выброса гонадропинов из гипофиза. У женщин при высоких дозах могут наступить андрогеннообусловленные явления маскулинизации: снижение тембра голоса (часто необратимое), усиленное оволосение, акне, повышенное либидо, иногда гипертрофия клитора.
Дианабол (действующее химическое вещество метандростенолон/метандиенон), торговые названия - анабол, нерабол, диалон и др., оральный стероид, оказывающий сильное воздействие на белковый обмен ("стероид мышечной массы"). Под его влиянием усиливается синтез белков, эффект выражается в положительном балансе азота в организме и в улучшении общего состояния организма. Дианабол способствует поступлению кальция в костную ткань. Показан при заболеваниях, когда необходимо анаболическое и общеукрепляющее воздействие.
Дианабол может вызывать желудочно-кишечные расстройства. У женщин он ведет к заметным явлениям маскулинизации, поэтому едва ли дианабол показан им. В высоких дозировках и при длительном применении дианабол действует токсично на печень. В связи с тем, что дианабол быстро повышает вес посредством сильной аккумуляции воды, возможны повышение давления и тахикардия. Дианабол в высокой степени ароматизирован и легко превращается в эстрогены, вызывая у некоторых лиц гинекомастию и ухудшает и без того плохое состояние. Он может вызвать акне на лице, шее, груди, спине и плечах, т.к. стимулирует деятельность сальных желез. У лиц с наследственной предрасположенностью дианабол может ускорить облысение, причиной чего является высокая превращаемость его химического вещества в дигидротестостерон. В силу значительного влияния на уровень эндогенного тестостерона он сокращает уровень выработку тестостерона в организме на 30-40 %, чем объясняется ярко выраженный антигонадотропный эффект. По мере прекращения приема препарата часто наблюдается потеря силы и мышечной массы, т.к. скопленная во время приема препарата в организме вода вновь выводится из него. При приеме в высоких дозах иногда наблюдается нарастающее агрессивное поведение человека. Поэтому у людей "взрывного" характера его прием может привести к неконтролируемым действиям.
Тем не менее дианабол является для большинства спортсменов анаболиком "хорошего самочувствия", способствуя и психологическому просветлению и повышающейся самооценке.
Особенно характерны побочные эффекты при приеме дианабола отечественного производства, при его употреблении отмечаются какие- то странные, выходящие за рамки обычной нормы, побочные явления с вариациями от дурноты, рвоты до настоящих заболеваний, которые приковывали не одного спортсмена к постели на несколько дней. Но главное отличие его в том, что препарат сильно влияет на печень.
Дураболин (действующее химическое вещество – нандролонфенилпропионат), торговые названия – активин, дуролон, феноболин и др., довольно похож на очень популярный Дека-дураболин и его предшественник. Но если дека-дураболина достаточно одной недельной инъекции, то дураболин требует частых и регулярных инъекций. Дураболин более подходит для подготовки к соревнованиям, в то время, как дека имеет преимущество в накоплении силы и массы.
Дураболин относится к надежнейшим и безопаснейшим стероидам, который между тем обладает довольно благоприятным воздействием. Побочные эффекты возникают в очень редких случаях и у особо чувствительных людей. Возможны явления маскулинизации у женщин, как хрипота голоса, снижение тембра голоса, гирсутизм, акне, повышенное либидо, но как правило, они развиваются при приеме высоких дох препарата. Эсиклен (хубернол), действующее химическое вещество – формсболон, является стероидом, хотя и отличается от остальных стероидов, он мало пригоден с точки зрения его анаболического воздействия. В месте его инъекции развивается локальное воспаление мышечной ткани, задействованная мышца опухает и увеличивается в размерах. Поэтому препарат применяется спортсменами бодибилдинга, как правило, в последние 7-14 дней перед соревнованиями, чтобы привести в надлежащий вид ту или иную мышечную группу: бицепс, трицепс, задняя дельтовидная мышца, икроножная мышца.
Препарат хорошо переносится, за исключением болей в месте инъекции, да в некоторых случаях слегка припухших мышц, других значительных отрицательных сопровождающих явлений эсиклен не имеет.
HCG, человеческий хориогонадотропин (действующее химическое вещество: хориогонадотропин), торговые названия: A.P.L., биогонадил, хорагон, хорион плюс, глюкор, гонадотрафон, прегнил и др. является не анаболическим/андрогенным стероидом, а естественным гормоном, который образуется в плаценте беременной женщины.
HCG обладает почти такими же качествами, что и лютеинизирующий гормон, поэтому инъекционный HCG используется для усиленной выработки тестостерона. Обычно спортсмены употребляют HCG для смягчения негативных явлений, появляющихся при прекращении приема стероидов, принимаемых длительное время.
Спортсмены обычно принимают HCG в конце стероидного курса, чтобы не "сломаться", т.е. чтобы обеспечить себе лучший переход к "естественным тренировкам".
У многих штангистов, спортсменов бодибилдинга при приеме препарата снижается сексуальный интерес в конце тяжелого цикла тренировок, незадолго до и сразу после состязаний и особенно в конце стероидного курса.
Прием HCG может вызвать те же побочные явления, что и прием тестостерона. При повышенной выработке тестостерона повышается и уровень эстрогенов, результатом чего может стать гинекомастия (рост молочных желез). У мужчины наблюдается заметный рост груди. В высоких дозах препарат может стать и причиной появления угрей, а также причиной аккумуляции в организме воды и минеральных солей. У очень молодых спортсменов HCG, как и анаболические стероиды, может привести к преждевременному завершению роста кости.
HCG считается недопустимым допингом в соревнованиях и на него проводятся допинг-контроли.
Лазикс (действующее химическое вещество – фуросемид) является диуретиком и используется с целью снизить массу тела за счет интенсивного обезвоживания организма. Так, спортсмены бодибилдинга принимают лазикс незадолго перед соревнованиями, чтобы в момент соревнований выглядеть на сцене упругими, поджарыми.
К побочным эффектам лазикса относятся нарушения деятельности системы кровообращения, появляются головокружения, обезвоживание, мышечные спазмы, рвота, сосудистый коллапс, поносы, чувство недомогания.
Может наступить остановка сердца.
Нольвадекс (действующее химическое вещество - тамаксифенцитрат) не относится ни андрогенным, ни анаболическим средствам, он принадлежит к группе сексуальных гормонов и является анти-эстрогеном. В норме сфера его применения - лечение определенных форм рака груди у женщин. Нольвадекс принимают одновременно с анаболическими стероидами, так как действие большинства стероидов может повысить уровень эстрогенов в крови с явлениями феминизации (гинекомастия, усиленное накопление жира и повышенное скопление воды в организме), а анти-эстроген нольвадекс противодействует этому. Но в редких случаях, к сожалению, нольвадекс не понижает уровень эстрогенов, а может наоборот повысить. Препарат ослабляет анаболическое действие некоторых стероидов.
Среди побочных эффектов наблюдается рвота, повышение температуры тела, помрачение сознания, оцепенелость, нарушения зрительной функции, а у женщин могут наблюдаться нарушение менструального цикла, что проявляется в скудных менструациях или вообще в их отсутствии.
Омнадрен 250 (действующие химические вещества –тестостеронфенилпропионат) - четырехкомпонентный препарат тестостерона.
Омнадрен применяется в пауэрлифтинге и бодибилдинге исключительно для наращивания силы и массы тела, как правило, за счет скопления воды в мышцах. Препарат характеризуют как "Омна-череп" (за счет пастозности лица, что заметно на щеках, лбу, под глазами).
Побочные явления сходны с таковыми у других препаратов тестостерона, наиболее характерны наряду с задержкой жидкости появление угрей и повышенная агрессивность.
Параболан (действующее химическое вещество - тренболон гексагидробензилкарбонат), относительно молодой стероид. В бодибилдинге и пауэрлифтинге это один из наиболее предпочтительных препаратов. Параболан - сильный андрогенный стероид, в нем также выражено высокое анаболическое качество. Параболан дает принимающим его необычный прирост силы, который особенно ярко выражен при приеме его в сочетании с оксандролоном. Так как параболан не нарушает водный обмен, не происходит никакого резкого увеличения веса, зато характерен качественной прирост мускулатуры.
Параболан довольно токсичен, оказывая влияние в первую очередь на почки, затем на печень. Спортсмены, принимающие его в высоких дозах и свыше нескольких недель, часто отмечают необычно сильное потемнение мочи. В отдельных случаях в моче может появиться кровь. Наряду с этим у многих спортсменов проявляется агрессивное поведение, причиной чего является сильное андрогенное действие препарата. Вместе с тем по сравнению с другими препаратами акне и выпадение волос очень редки. По мере прекращения приема препарата наблюдается отчетливый спад силы, в то время как наращенная мускулатура сохраняется дольше.
Провирон (действующее химическое вещество: мастеролон) - синтетический, орально действующий андроген, не обладающий анаболическими свойствами. В медицине применяется при лечении нарушений, вызванных недостатком мужских половых гормонов. Поэтому многие спортсмены применяют его в конце стероидного курса для поднятия сниженной выработки тестостерона.
Побочные эффекты провирона у мужчин при приеме небольших доз препарата крайне редки. При высоких дозировках может привести к задержке в организме электролитов и воды, к развитию отеков. Наиболее частое побочное явление провирона - выраженная сексуальная суперстимуляция и в отдельных случаях длительная эрекция. Это состояние болезненно и может повлечь за собой всевозможные нарушения, при его появлении имеет смысл снизить дозу препарата либо вообще прекратить прием препарата. Женщины должны с осторожностью принимать провирон, т. к. не исключены всевозможные андрогенные побочные явления.
Сустанон 250 (действующее химическое вещество – тестосиберонпропионат, смесь четырех тестостеронов) - очень популярный стероид, в сравнении с другими препаратами тестостерона, имеет несколько преимуществ: начинает действовать быстро и в то же время остается эффективно действующим в организме в течение нескольких недель. Он обладает выраженным андрогенным воздействием, которое сочетается с сильным анаболическим эффектом. Пригоден для наращивания силы и мышечной массы, не задерживая воду в организме.
Побочные явления похожи с побочными эффектами тестостеронэнантата, хотя они проявляются менее часто и не так сильно выражены. В зависимости от времени приема и доз сустанона могут наблюдаться обычные андрогеннообусловленные побочные явления, такие, как акне, агрессивность, сексуальная суперстимуляция, отложение жира в коже, ускоренное выпадение волос, сниженная выработка половых гормонов.
Тестостерон энантат (действующее химическое вещество - тестостерон энантат, в США существуют еще 14 препаратов, содержащих действующее химическое вещество тестостерон энантат) - сложный эфир естественного тестостерона. Он отвечает за нормальное развитие мужских половых признаков. В медицине тестостеронэнантат находит применение: у мальчиков и подростков применяется при терапии роста, а у женщин находит применение в качестве дополнительного лечения при определенных формах опухоли молочных желез в постменструальный цикл.
Тестостеронэнантат – стероид длительного действия, обеспечивающий долгую продолжительность воздействия на организм. В зависимости от обмена веществ и гормональной системы действие препарата - 2 - 3 недели, так что теоретически возможны очень большие интервалы между инъекциями. Его применяют в бодибилдинге, троеборье и в тяжелой атлетике раз в неделю. Основным преимуществом тестостеронэнантата является очень сильный андрогенный эффект и интенсивное анаболическое действие, поэтому с его помощью в кратчайшее время достигается эффект в увеличении силы и массы тела. Тестостеронэнантат очень сильно стимулирует процессы регенерации в организме, поэтому он быстро действует в отношении повышения жизненного тонуса, прилива энергии и ускорения фаз компенсации. Но уже через 2 недели после отмены препарата кожа теряет свою рельефность, становится гладкой, плоской, мускулатура отечной. Она выглядит так, будто бы надута воздухом. Так выглядят "чемпионы бодибилдинга" в межсезонье и в период наращивания массы.
Начинающим в стероидных курсах следует избегать всех видов тестостеронов, использовать "более легкие" стероиды.
При высокодозированной терапии тестостерон-препаратами часто наблюдается прекращение или снижение сперматогенеза. Поэтому побочные явления тестостеронэнантата - это, прежде всего явления, вызванные его сильным андрогенным воздействием и повышенным скоплением воды в организме. Как правило, они и являются причиной часто возникающей при приеме тестостеронэнантата гипертонии. Довольно часто прием препарата сопровождается появлением распространенных угрей на спине, груди, плечах, руках, чуть меньше на лице, причем чаще сыпь появляется не во время приема тестостеронэнантата, а после прекращения приема. Другое побочное действие - проявляющаяся в начале приема препарата сексуальная суперстимуляция с частыми эрекциями. Тестостерон может привести к ускоренному росту и созреванию костной ткани, к преимущественному наращиванию эпифизов, а, следовательно, к прекращению процесса poста тела. К побочным эффектам относится атрофия яичек, сниженный сперматогенез, а также повышенная агрессивность. Большие дозы могут стать причиной стероидных психозов - "психозы мегадоз андрогенов". К побочным явлениям относятся также снижение тембра голоса и ускоренное выпадение волос, причем изменения в голосе и алопеция необратимы, гирсутизм и гипертрофия клитора обратимы лишь частично. Тестостерон пропионат (действующее химическое вещество - тестостеронпропионат) - сложный эфир тестостерона, в отличие от длительно действующих тестостерона энантата и ципионата, пропионат имеет значительно более короткую продолжительность воздействия. В силу сильного андрогенного действия пропионат, также как и энантат и ципионат предназначен для наращивания силы и массы тела. Показан женщинам, т.к. при правильном его применении можно избежать андрогеннообусловленных побочных явлений.
Тестостеронпропионат обычно применяется непосредственно перед соревнованиями в качестве "терапии страха", если нужно успешно пройти допинг-контроль.
Хотя побочные явления пропионата и похожи на побочные явления энантата, они проявляются реже. При генетической предрасположенности препарат в очень высоких дозах может вызвать известные андрогеннообусловленные побочные эффекты: акне, выпадение волос, усиленное оволосенение на теле, снижение тембра голоса. Повышенное либидо часто наблюдается как у мужчин, так и у женщин. Гинекомастия несмотря на высокий уровень конвертируемости пропионата проявляется реже, чем при приеме других тестостеронов. Возможна задержка воды в организме.
Гормон роста (действующее химическое вещество - соматропин), торговые названия: крескормон, гуматроуп, нордитропин применяется для продолжительного наращивания мышц. Это самый большой риск, на который может пойти спортсмен, так как побочные явления необратимы. Гормоны роста окружены в своем использовании и применении аурой таинственности, одни называют его чудо средством, которое в кратчайшее время дает гигантский прирост силы и массы, другие считают его полностью бесполезным в достижении спортивных результатов и объясняют это тем, что препарат стимулирует рост только отстающих в физическом развитии детей.
Гормон имеет сильный анаболический эффект и способствует повышенному синтезу белков, что выражается в мышечной гипертрофии и в гиперплазии мышц. Последнее выражено довольно интересно, стероиды подобным эффектом не обладают, поэтому соматотропный гормон называют самым сильным анаболическим гормоном. Во-вторых, соматотропный гормон оказывает сильное влияние на процесс сжигания жира, превращая жир в энергию, что ведет к интенсивному его исчезновению.
Соматотропный гормон укрепляет соединительную ткань, сухожилия, кости и хрящи, что, вероятно, и является одной из главных причин неимоверного прироста силы, который наблюдается у некоторых спортсменов. По оценкам некоторых спортсменов бодибилдинга и пауэрлифтинга, соматотропный гормон защищает благодаря последнему качеству от повреждений, если при одновременном приеме стероидов сила стремительно растет.
Но, при применении гормона повышается потребность организма в гормоне щитовидной железы, инсулине, кортикостероидах, гонадотропинах, эстрогенах, андрогенах и анаболиках. Это и является причиной того, что соматотропный гормон как единственно принимаемый препарат значительно менее эффективен и может оказывать свое оптимальное воздействие на организм лишь при дополнительном приеме стероидов, гормона щитовидной железы и инсулина. А это уже суммация побочных эффектов.
Соматотропный гормон вызывает побочные явления, не схожие с эффектами стероидов. Основная проблема - это возможный недостаток сахара в крови или возможная гипофункция щитовидной железы. Акромегалия, диабет, гипертрофия миокарда, высокое артериальное давление, рост почек и печени могут теоретически возникнуть при излишнем и долгом приеме гормона роста. Но на практике они редки. Более частые проблемы с соматотропным гормоном возникают тогда, когда спортсмен дополнительно вводит инсулин.
Винстрол депот (действующее химическое вещество – станозолол) по оценкам некоторых специалистов «во всех отношениях полностью бесполезен. В обычных традиционных дозах винстрол на обладает побочными явлениями, достойными упоминания, но в любой дозе он не способствует ни заметному наращиванию мышц, ни приросту силы. Женщинам он также малополезен, как и мужчинам» (Кзрр Р., 1999). Главная область применения винстрола длительного действия – бодибилдинг в период подготовки к соревнованиям. В сочетании с ограниченной в калориях диетой, которая богата белками, винстрол длительного действия придает мускулатуре твердость и упругость.
К побочным эффектам препарата относится образование рубцов в месте его инъекций, т.е. на ягодицах, что заставляет вводить винстрол в плечи, ноги или даже в икроножные мышцы.
Прививочные реакции на вакцины могут быть как локальные, так и общие. Чаще встречаются местные реакции небольшой степени выраженности, но иногда развиваются инфильтрация, выраженный отек, сильна болевая реакция. Характерно повышение температуры тела, у больных появляются боли в суставах, высыпания в виде крапивницы, ринит, бронхоспазм и в тяжелых случаях - анафилактический шок.
Наиболее частой причиной развития аллергических реакций являются примеси. Так, к примеру, белки яиц, присутствующие в вакцинах, выращенных на куриных или иных эмбрионах у лиц с наличием аллергии к белку обусловливают развитие системных проявлений. Имеет значение наличие консервантов, добавленных в сывороточный материал (антибиотики, формальдегид, метиолят).
В пятидесятые годы, в нашей стране гомеопатия была запрещена вместе с генетикой, кибернетикой, и традиционная медицина отрицала ее достижения. Сейчас гомеопатия стала полноправным разделом медицины, ее использование разрешено официальным приказом министерства здравоохранения, курсы гомеопатии преподают в медицинских институтах, в институте повышения квалификации врачей. После обучения врач получает сертификат специалиста установленного образца, и каждые 5 лет, как и в других областях медицины, подтверждает свою квалификацию на экзамене.
Так как гомеопатия стала частью лекарственной терапии населения, нельзя обойти молчанием и возможные побочные реакции и осложнения при приеме гомеопатических средств, хотя этот раздел изучен еще меньше, чем побочные реакции и осложнения традиционной медицины.
Гомеопатические препараты делятся на насколько больших групп – растительные, животные, минералы, кислоты и соли, продукты пораженного организма. Растительные препараты обычно это первая помощь, показаны в острых ситуациях, они действуют быстро, недолго, поэтому принимать их рекомендуют часто. Металлы и препараты остальных групп начинают действовать не сразу, иногда через несколько дней. Действие их глубже и длится дольше, они часто влияют не на отдельный орган, а на весь организм. Как первая помощь применяются редко.
Гомеопатическим лекарство делает способ его приготовления, а исходным веществом может быть что угодно – от поваренной соли (Натриум муриатикум) до чернил каракатицы (Сепия).
Дозы гомеопатических препаратов называются “разведениями” и бывают десятичными или сотенными. Десятичные разведения готовятся так: к одной части лекарства добавляется 10 частей воды, перемешивается и встряхивается для равномерного распределения действующего вещества в растворе. Получается первое десятичное разведение. Потом одну часть этого раствора соединяют с 9 частями воды, перемешивают и встряхивают – это второе десятичное разведение, и т. д. При приготовлении сотенных доз, технология та же, но к одной части вещества добавляется 99 частей воды. Минимальным используемым разведением является 3Х – третье десятичное разведение, максимальными – тысячные сотенные разведения. Интересно, что в разведениях больше С12 (12-го сотенного) уже нет молекул действующего вещества, работает только энергия, “память” воды.
В аптеках страны помимо лекарств московской фармацевтической фабрики есть множество гомеопатических препаратов фирм “Веледа”, HELL, DHY, BIONORICA, WALSH PHARMA. Это, как правило, композиты, содержащие большое количество лекарственных веществ в разных разведениях, подобранных таким образом, чтобы оказывать лекарственное воздействие на каждого употребляющего препарат. Побочные действия при их приеме крайне редки, показания – широки.
Как и для любого метода, границы применения гомеопатии существуют и определяются многими факторами.
Вот как характеризует гомеопатию в Интернет один из врачей ассоциации. «При приеме идеально подобранного гомеопатического препарата, полностью соответствующего конституции человека, происходит коррекция, нормализация работы всех органов и систем организма. Сначала болезнь покидает “центр” тела, потом уходит и с “периферии”. По существующему в гомеопатии согласно правилу Геринга излечение идет изнутри кнаружи и сверху вниз, например, сыпь исчезает сначала с головы, потом с тела, и уже после этого с конечностей. Если у больного бронхиальной астмой после приема препарата прошли приступы но появились кожные высыпания – это правильный процесс излечения, а если прошли приступы, но появились головные боли – значит, лекарство подобрано неверно, оно загоняет болезнь внутрь организма и требуется смена препарата. Лекарственное обострение – не необходимый, но и не опасный промежуточный этап лечения, оно не угрожает жизни больного и проходит самостоятельно. Впрочем, если терпеть это очень неприятно, можно дополнительными гомеопатическими средствами облегчить его протекание. Чаще лекарственное обострение возникает при приеме конституционального препарата, того единственного, который корректирует работу организма в целом. При таком методе лечения человек, возможно, за короткое время переболеет всеми болезнями, которые он “заглушил”, “забил” лекарствами, и которые, поэтому, не выполнили свою работу в организме, не укрепили его иммунную систему. Болезни эти “проживаются” от более свежих, недавних, к детским, каждая продолжается несколько дней, и проходит без лечения и без нежелательных последствий. При лечении “комплексонами” – лекарствами, составленными из нескольких препаратов, наиболее подходящих данному человеку от конкретной патологии – обострения крайне редки.
Так как гомеопатия более тонкий и индивидуальный метод лечения, чем аллопатия, и подбор лекарства, являющегося конституциональным для данного больного, требует высочайшей квалификации врача, хороших специалистов по такому лечению мало. Много врачей, назначающих сборы из препаратов - “комплексоны” или “композиты”. Этот метод менее индивидуальный, но тоже действенный. Наконец, в аптеках без рецепта продают готовые гомеопатические сборы – от болезней горла, от простуды, менструальных болей, снимающий тягу к спиртному и многие другие. Такие лекарства содержат в своем составе много препаратов в разных разведениях и помогают всем, хотя бывают недостаточно эффективны для конкретного больного».
Подобная характеристика действия гомеопатических средств свидетельствует лишь о том, что научная медицина еще не стала базой в гомеопатии. Поэтому и оценка побочных эффектов – дело будущего.