ОСТРЫЕ ЛЕЙКОЗЫ
Классификация. Этиология. Патогенез.
А.В.Колосков
(лекция для врачей и студентов)
Под термином "острые лейкозы" понимают группу клональных заболеваний, первично возникающих в костном мозге в результате мутации стволовой клетки крови. Следствием мутации является потеря потомками мутировавшей клетки способности к дифференцировке до зрелых клеток крови.
Группу острых лейкозов объединяет общий морфологический признак: субстрат опухоли представлен незрелыми молодыми клетками -- бластами. Классификация острых лейкозов основана на признаках принадлежности опухолевых клеток к тому или иному ростку гемопоэза. Принадлежность опухолевых клеток может быть определена цитохимическим методом на основании выявления в цитоплазме этих клеток специфических включений (например гликогена в клетках лимфоидного ростка гемопоэза, миелопероксидазы в клетках миелоидного ростка гемопоэза или альфа-нафтилэстеразы в клетках моноцитарного ряда). Кроме того, для определения гистогенеза опухолевых клеток используется иммунологический метод (иммунофенотипирование), выявляющий на цитоплазматической мембране клетки антигены (кластеры дифференцировки -- CD), указывающие на происхождение клетки и степень ее зрелости.
На сегодняшний день для практических и научно-исследовательских целей используется Франко-Америко-Британская (FAB) классификация острых лейкозов. Классификация подразделяет все острые лейкозы на две главные подгруппы -- острые нелимфобластные лейкозы (составляют около 70% всех острых лейкозов) и острые лимфобластные лейкозы (составляют 30% всех острых лейкозов).
Для разграничения различных вариантов острых лейкозов (ОЛ) FAB классификация использует ряд цитологических критериев аспирата костного мозга и мазка периферической крови, а также цитохимические тесты.
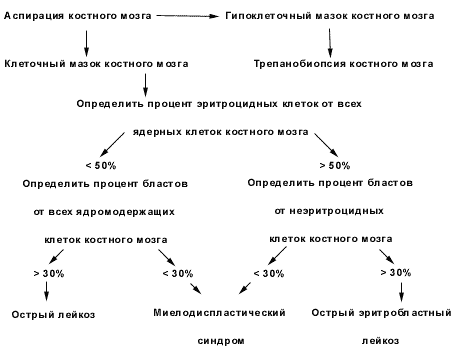
Первым шагом FAB классификации является разграничение ОЛ и миелодиспластического синдрома, а также выделение острого эритробластного лейкоза (для его обозначения FAB классификация использует символ -- М6) (рисунок 1).

Рисунок 1. Алгоритм для диагностики острых лейкозов и разграничения их с миелодиспластическим синдромом. (по Bennett J.M. et al., 1985).
Далее для на основании цитологических и цитохимических критериев FAB классификация выделяет следующие варианты ОНеЛЛ (по Bennett J.M. et al., 1985).
Острый миелобластный лейкоз (М1)
Аспират костного мозга:
Острый миелобластный лейкоз с частичным созреванием (М2)
Аспират костного мозга:
Острый промиелоцитарный лейкоз (М3)
Этот вариант ОНеЛЛ устанавливают на основании типичного морфологического субстрата (характерного вида промиелоциты в аспирате костного мозга) без использования каких-либо дополнительных тестов.
Острый миеломонобластный лейкоз (М4)
1. Аспират костного мозга:
- клетки миелоидного ростка кроветворения составляют не менее 30%, но менее 80%.
2. Периферическая кровь:
- клетки моноцитарного ростка кроветворения составляют не менее 5.0 х 10^9/л;
Острый монобластный лейкоз (М5)
Аспират костного мозга:
-- клетки моноцитарного ряда гемопоэза составляют не менее 80%.
Острый мегакариобластный лейкоз (М7) -- диагноз устанавливают на основании данных электронно-микроскопического исследования бластных клеток или на основании данных иммунофенотипирования.
Острый ранний миелобластный лейкоз (М0) - диагноз устанавливают на основании отрицательных результатов всех цитохимических окрасок бластных клеток или на основании данных иммунофенотипирования.
Для классификации ОЛЛ FAB классификация использует цитологические особенности бластных клеток. На основании этих признаков проводится подразделение на три варианта - L1, L2 и L3. Однако такое классификационное построение оказалось условным. Выделенные варианты реально не отличались по особенностям течения, длительности выживания больных и ответу на терапии, что послужило основанием для отказа от этой части FAB классификации. В настоящее время используются иммунофенотипическая классификация ОЛЛ, которая выделяет три основное группы:
Эпидемиология.
Ежегодно регистрируется 35 новых случаев острых лейкозов на 1 млн населения. Структура встречаемости острых лейкозов в значительной степени зависит от возраста. Так в возрастной группе до 15 лет соотношение ОЛЛ : ОНеЛЛ составляет 4 : 1, в возрастной группе от 15 до 35 лет - 1 : 1.5, а в возрастной группе старше 35 лет - 1 : 8. Мужчины и женщины болеют с одинаковой частотой.
Этиология.
Для острых лейкозов, как и для большинства других опухолевых заболеваний, невозможно выделить специфический этиологический фактор. Этиологические факторы, способные вызывать развитие опухоли, были подробно рассмотрены в главе "Хронические миелопролиферативные заболевания".
Патогенез.
В основе патогенеза острых лейкозов лежит мутация стволовой клетки крови, что влечет за собой практически полную потерю потомками мутировавшей клетки способности к созреванию. Мутантный клон автономен от каких-либо регулирующих воздействий организма и достаточно быстро вытесняет нормальные гемопоэтические клетки, замещая собой весь гемопоэз.
С момента мутации до момента появления клинических и лабораторных признаков заболевания проходит в среднем 2 месяца. За этот период времени количество опухолевых клеток увеличивается с 1 (родоначальница мутантного клона) до 10^9 -- 10^12. Масса такого количества клеток составляет около одного килограмма. Вытеснение нормальных гемопоэтических клеток, и замещение их опухолевыми клетками, неспособными к созреванию, закономерно приводит к уменьшению в периферической крови зрелых клеток с развитием анемии, гранулоцитопении, лимфопении, моноцитопении и тромбоцитопении, что будет проявляться соответствующей клинической картиной.
Уменьшение количества эритроцитов влечет за собой развитие анемического синдрома. Уменьшение или полное исчезновение зрелых гранулоцитов, приводит к развитию иммунодефицита и инфекционных осложнений. Свой вклад в патогенез инфекционных осложнений вносят также лимфопения и моноцитопения. Тромбоцитопения лежит в основе кровоизлияний и кровотечений.
В ряде случаев опухолевые клетки не нуждаются в строго необходимом для нормальных гемопоэтических клеток стромальном микроокружении. Они могут покидать костный мозг и образовывать колонии опухолевого гемопоэза в других органах и тканях (селезенке, лимфоузлах, печени, центральной нервной системе, легких, коже, слизистых оболочках). Инфильтрация опухолевыми клетками органов и тканей относят к проявлениям пролиферативного синдрома. Степень злокачественности опухолевых клеток при остром лейкозе с течением времени возрастает (как и для других групп опухолей, для острых лейкозов правомочен закон опухолевой прогрессии). Поскольку опухолевые клетки при острых лейкозах, в большинстве вариантов, изначально имеют выраженный дефект созревания, то большая злокачественность часто проявляется появлением экстрамедуллярных очагов кроветворения, увеличением пролиферативной активности, развитием резистентности к проводимой терапии. В основе озлокачествления лежат вторичные мутации в опухолевых клетках. Это наглядно демонстрируют результаты цитогенетического исследования, выявляющего на ряду с изменениями хромосом, имевшими место в начале заболевания, появление дополнительных поломок по мере течения заболевания.
В дебюте острых лейкозов хромосомные аномалии выявляют в 90% случаев. Однако, столь же часто выявляемой хромосомной поломки, как транслокация 9;22 (филадельфийская хромосома) при хроническом миелолейкозе, при острых лейкозах не наблюдается. Тем не менее известна связь некоторых перестроек хромосом с вариантом острого лейкоза. Так транслокация 15;17 является специфичной для острого промиелоцитарного лейкоза (М3), она выявляется в среднем в 50% случаев. Транслокация 8;21 чаще всего встречается при остром миелобластном лейкозе (М1). В трети случаев общего варианта ОЛЛ встречается транслокация 9;22 (филадельфийская хромосома). Клоны клеток с аномалией хромосом не определяются в период ремиссии и появляются вновь при развитии рецидива заболевания. Наиболее часто встречающиеся при острых лейкозах поломки хромосом представлены в таблице 1.
Таблица 1. Наиболее частые аномалии хромосом при острых лейкозах.
хромосомная аномалия вариант острого лейкоза
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Таким образом, в основе патогенеза острых лейкозов лежит мутация стволовой клетки крови. Следствием мутации является развитие в костном мозге клона клеток, утративших способность к созреванию. Неопластический клон вытесняет нормальные гемопоэтические клетки, что приводит к развитию дефицита зрелых клеток в периферической крови. Снижение количества или полное отсутствие зрелых клеток периферической крови приводит к выпадению соответствующих функций периферической крови, что влечет за собой развитие клинических проявлений заболевания. Патоморфология костного мозга.
В гистологическом препарате костного мозга при острых лейкозах определяется значительное увеличение количества бластных клеток, которые часто заполняют весь препарат.