Статья, которая вскоре будет опубликована в журнале ЗППП (Заболевания, Передаваемые Половым Путем)
Исследование липидной фракции клеточных взвесей T.pallidum и биологических жидкостей больных сифилисом.
Детектирование по стеринам.
Осипов Г.А.*1, Аковбян В.А.**, Бойко Н.Б.*, Киселева Г.А.**
*Академическая группа академика РАМН Ю.Ф.Исакова
** Центральный научно-исследовательский кожно-венерологический институт Минздрава РФ
1 Переписка с этим автором по адресу:
103001 Москва, Садово-Кудринская, 15
Детская городская клиническая больница им.Н.Ф.Филатова
Академическая группа академика РАМН Ю.Ф.Исакова
Тел. /095/ 254 6740; Факс: /095/ 254 1039; Электронная почта: osipovga@rusmedserv.com
Ключевые слова: сифилис, Treponema pallidum, бледная трепонема, диагностика, микробные маркеры, стерины, хромато-масс-спектрометрия
Резюме. Исследован состав липидной фракции клеточных взвесей T.pallidum, крови и других биологических жидкостей больных сифилисом. В качестве контроля использованы аналогичные данные доноров и соматических больных. Состав жирных кислот и альдегидов спирохеты повторяет состав клеток организма-хозяина. Заметные изменения найдены в метаболитах холестерина, которые могут быть использованы в качестве диагностических признаков. Составлена программа детектирования возбудителя по стеринам в крови и других биологических жидкостях человека методом хромато-масс-спектрометрии в режиме селективных ионов. Концентрации метаболитов оказалась достаточно высокой для диагностики заболевания сифилисом методами газовой или жидкостной хроматографии.
Введение
Система серологической диагностики сифилиса основана на обнаружении в крови антител к возбудителю заболевания - Treponema pallidum [1,6]. Фактически это означает, что с помощью известной лабораторной техники определяется некий продукт, образовавшийся в результате взаимодействия патогена и организма человека. Процесс этот достаточно сложен и мало изучен и зависит как от биологических свойств возбудителя, так и от реактивности организма. До настоящего времени мы не можем дать однозначного объяснения причин феномена серорезистенции и различия в сроках негативации у больных одинаковыми формами сифилиса, получивших однотипное лечение, достоверно определить инфицирование новорожденного от матери, переболевшей сифилисом, и т.д. В значительной степени ответы на эти и многие другие вопросы могли бы быть получены при условии идентификации в крови или других биологических жидкостях человека самого возбудителя или каких-либо специфических компонентов (маркеров). До настоящего времени эта задача представлялясь трудноразрешимой.
В ряде последних сообщений [2-6] достаточно полно отражено общее состояние лабораторной [2] и текущие аспекты клинической диагностики сифилиса [3-6]. Традиционно используемыми методами являются микроскопия в темном поле, метод иммунофлуоресценции [6] и биологический метод (испытание на кроликах) [4], хотя первичную информацию можно получить с помощью простых и недорогих тестов, использующих липидные антигены [2].
Биологический метод очень чувствителен и специфичен, нo требует значительных затрат времени, метод микроскопии нуждается в хорошей технике и высококвалифицированных специалистах (субъективен), а серологический тест недостаточно чувствителен при ранней инфекции.
Для достижения наилучших диагностических результатов необходимо совершенствовать имеющиеся методы и развивать новую технику. Перспективным направлением, использующим молекулярные методы детектирования, является реакция полимеразного связывания (PCR) и лигандного связывания (LCR), которые обладают повышенной чувствительностью обнаружения T.pallidum [3]. Техника PCR успешно использована для для доказательства присутствия Т.pallidum при вторичном и первичном сифилисе [4], когда обычные методы не работают из-за деградации или отсутствия трепонемальной спирохеты на поздней стадии сифилитической язвы. Описан высокочувствительный и специфичный вариант PCR (100 клеток возбудителя) - полимеразной цепной реакции с обратной транскрипцией (RT-PCR). Чрезвычайно эффективен сложный PCR (M-PCR) - анализ с колориметрическим детектированием для одновременной амплификации ДНК-участков трех микроорганизмов: Haemophylus ducrey, T.pallidum и вируса герпеса в пробах из генитальных органов [8]. Результаты оценки 298 образцов и сравнение их с микроскопическим исследованием, а также результатами культивирования на двух средах показали значительные преимущества данного метода по чувствительности по сравнению с традиционными. Однако сравнение метода флуорecцентных антител и метода PCR на 156 образцах от пациентов с с генитальными язвами показало, что эти методы эквивалентны при выявлении инфекции [9]. Применение перспективного метода твердофазного ферментного иммуноанализа для диагностики раннего сифилиса [10] показало, что он может служить альтернативой традиционным методам, хотя менее чевствителен и специфичен. Заслуживают внимания данные применения антенатального (утробного) сканирования при диагностике материнского сифилиса [11].
Тем не менее, несмотря на обнадеживающие результаты по применению новых перспективных методов и диагностики сложных случаев конгенитального и нейросифилиса [2,4,7,13], разработка экспрессных методов диагностики раннего, вторичного и третичного сифилиса остается актуальной проблемой. Так, диагностическая ценность PCR как возможного альтернативного метода еще недостаточна. Дискутируется также вопрос, сможет ли ферментный иммуноанализ полностью заменить или лишь дополнит существующие традиционные методы [5]. На этом фоне выглядят интересными новые комплексные подходы в диагностике сифилиса на основе высокочувствительного и объективного хроматографического метода исследования [12], а также его комбинации с масс-спектрометрией, который эффективно используется для диагностики других видов инфекции [14,15]. Последний, судя по публикациям, позволяет достичь желаемого результата - определять присутствие самого возбудителя по его специфичным компонентам: химическим составляющим клетки, собственным метаболитам или продуктам взаимодействия с клетками хозяина.
В настоящей работе представлены результаты исследования состава липидной фракции стандартного трепонемного антигена и лиофилизата взвеси бледных трепонем, а также биологических жидкостей (кровь, отделяемое вагины, эякулят, тканевый экссудат клапана сердца) у больных сифилисом, лиц, обратившихся в клиники ЗППП на обследование, соматических больных и доноров.
Материалы и методы.
Исследованы три препарата клеточных компонентов T.pallidum.
Препарат ТР-1. Взвесь в физиологическом растворе свежеполученных клеток спирохет из семенников инфицированного кролика.
Препарат ТР-2. Лиофилизат патогенных бледных трепонем штамма Никольса.
Препарат ТР-3. Лиофилизированный стандартный антиген спирохет, полученный на искусственной среде в заводских условиях (Ставрополь).
Исследован состав липидных компонентов - жирных кислот, спиртов, альдегидов и стеринов крови больных сифилисом, а также других биологических жидкостей пациентов, обратившихся в клинику ЗППП на обследование. В качестве контроля использованы данные анализа аналогичных биологических жидкостей пациентов гинеколога и уролога, соматических больных и доноров. Список проб приведен в табл.2.
Проба водной клеточной взвеси T.Pallidum стерилизована добавлением 2мл метанола перед напрвлением на анализ. Далее добавлен хлороформ до соотношения монофазной системы растворителей вода:метанол:хлороформ=1:1:0.9, применяемой для экстракции липидов. Экстракцию проводили в течение трех часов при периодическом инициировании на вибраторе Vortex. Затем добавляли воду и хлороформ до разделения фаз, двухфазную систему центрифугировали, нижнюю фазу (хлороформ) переносили пипеткой в чистые пробирки, упаривали досуха в токе инертного газа. Полученный таким образом экстракт липидов подвергали кислому метанолизу в 1N HCl в метаноле. Метанолиз проводили в 0.4 мл реактива течение часа при 80° С. На этой стадии происходит освобождение жирных кислот и альдегидов из сложных липидов. Липидную фракцию из реакционной смеси двукратно экстрагировали гексаном, высушивали и обрабатывали 20 мкл N,О-бис(триметил-силил)-трифторацетамида в течение 15 мин при 65 ° С для получения триметилсилильных эфиров окси-кислот. Реакционную смесь эфиров в количестве 1 мкл вводили в инжектор хромато-масс-спектрометра системы QP2000 фирмы Шимадзу (Япония). Для управления и обработки данных использовали штатные программы прибора. Хроматографическое разделение пробы осуществляли на капиллярной колонке. Для идентификации и количественного анализа компонентов проб использовали масс-спектрометр в режиме сканирования или масс-фрагментографии (МФ), при отработке диагностики Т.pallidum по выявленным маркерным веществам. Для этого введены дополнения в программу масс-фрагментографии, используемой для определения микробных маркеров в крови и других биологических жидкостях [15]. Интервалы и ионы выбирали таким образом, чтобы селективно детектировать эти маркеры на превалирующем фоне липидных компонентов субстрата. В качестве репера при количественных измерениях использована величина хроматографического пика гептадекановой кислоты, содержание которой постоянно в биологических жидкостях млекопитающих и составляет, по нашим измерениям, 20мкг/мл.
Результаты и обсуждение.
Анализ липидной фракции экстрактов из препаратов спирохет показал, что их жирнокислотный профиль составляют в основном четные насыщенные и ненасыщенные жирные кислоты, характерные для клеток млекопитающих (табл.1). Сравнение с составом ЖК крови человека показывает качественное совпадение данных, что cогласуется с известными данными об отсутствии у T.pallidum собственного аппарата синтеза липидов и их заимствованию из клеток хозяина [15]. Cостав жирных кислот патогенных трепонем штамма Никольса (ТР-1), извлеченного из семенников кролика, а также лиофилизата очищенного антигена, полученного лабораторным (ТР-2) и заводским (ТР-3) способами. одинаков. Изолят ТР-1 отличается большим содержанием холестерина и наличием полиненасыщенных кислот с числом атомов углерода 20 и 22, так как эта проба включает экссудат ткани кролика. Кроме холестерина в нем содержатся четыре метаболита, синтез которых может быть индуцирован под влиянием возбудителя. Три из них идентифицированы по масс-спектрам как кампестерол, ситостерол и этилкопростанол. Все новые стерины имеют специфические масс-спектры, удобные для их детектирования. Кроме них в клетках и взвесях спирохет не обнаружено других липидных компонентов, которые могли бы служить маркерами возбудителя на фоне биологических жидкостей человека.
Таблица 1.
Состав жирных кислот (% от суммы) препаратов антигена T.pallidum и крови человека
|
№ |
Вещество |
Вид антигена |
Кровь |
||
|
ТР-1 |
ТР-2 |
ТР-3 |
человека |
||
|
1 |
Миристиновая |
0,9 |
0,5 |
||
|
2 |
Пентадекановая |
0,3 |
0,6 |
0,1 |
|
|
3 |
Гексадеценовая |
2,6 |
0,5 |
0,8 |
0,9 |
|
4 |
Пальмитиновая |
27,5 |
40,9 |
30 |
11,2 |
|
5 |
Пальмитальдегид |
0,3 |
0,4 |
||
|
6 |
аи-Гептадекановая |
0,3 |
2,4 |
0,1 |
|
|
7 |
Гептадекановая |
0,4 |
0,5 |
0,6 |
0,2 |
|
8 |
Линолевая |
15 |
7,4 |
5,2 |
14,9 |
|
9 |
Олеиновая |
12,3 |
12,9 |
14,4 |
9,1 |
|
10 |
Стеариновая |
9,7 |
24 |
33,8 |
4,9 |
|
11 |
Олеиновый альдегид |
2,1 |
0,1 |
||
|
12 |
Стеаральдегид |
0,3 |
1,8 |
0,6 |
|
|
13 |
Нонадекановая |
0,3 |
|||
|
14 |
Арахидоновая |
0,5 |
1,3 |
1 |
|
|
15 |
Эйкозановая |
0,2 |
1,7 |
0,2 |
|
|
16 |
Докозагексеновая |
1,6 |
1,7 |
||
|
17 |
Докозапентеновая |
0,7 |
0,9 |
||
|
18 |
Докозановая |
0,5 |
0,2 |
||
|
19 |
Тетракозеновая |
0,4 |
1,4 |
||
|
20 |
Тетракозановая |
0,3 |
1,3 |
||
|
21 |
Гексакозановая |
0,2 |
0,1 |
||
|
22 |
Холестерин |
26,2 |
12,1 |
2,4 |
50,4 |
Экстракты липидной фракции крови и других биологических жидкостей больных сифилисом и здоровых доноров также совпадают по составу жирных кислот, но отличаются наличием у больных дополнительных метаболитов холестерина которые, видимо принадлежат продуктам взаимодействия клеток хозяина с возбудителем (интерактивные метаболиты). Среди них два, ситостерол и кампестерол, являются общими с метаболитами инфицированного T.pallidum кролика. Два оставшихся характерны только для человека. Один из них - тетраметилхолестерин, другой пока не идентифицирован, несмотря на использование самой последней библиотеки масс-спектров (78000 спектров) и сведений из периодической литературы. Для него будем использовать условное название “стерин 428”. Все стерины имеют четкие особенности масс-спектров, которые могут быть использованы при их детектировании методом ГХ-МС селективных ионов.
Три вещества 4b -метилхолестерол (кампестерол), b -ситостерол, и неизвестный М=428 выбраны для оценки диагностической значимости. Анализ проб биологических жидкостей проведен по модифицированнй программе масс-фрагментографии, используемой для определения микробных маркеров в крови и других биологических жидкостях [15]. Результаты приведены в таблице 2.
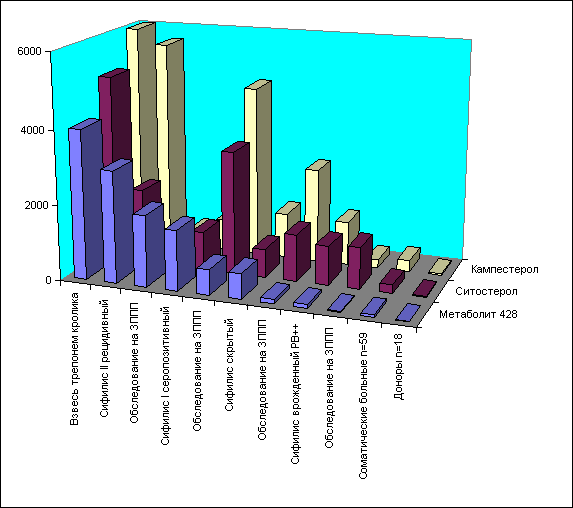
Как видно из этой таблицы и трехмерной диаграммы (рис.2), концентрация трех маркеров в пробах больных и лиц из групп риска значительно выше, чем у доноров и соматических больных.
Таблица 2.
Содержание избранных метаболитов холестерина у пациентов разных категорий и доноров
|
№ |
Код |
Диагноз |
Содержание маркеров, нг/мл |
Вид пробы |
||
|
пробы |
Метаболит 428 |
Ситостерол |
Кампестерол |
|||
|
1 |
Доноры |
Доноры n=18, максимальные значения |
6 |
32 |
40 |
Кровь |
|
2 |
Соматические больные n=59, максимальные значения |
60 |
230 |
300 |
Кровь |
|
|
3 |
VF-756 |
Обследование на ЗППП |
44 |
1110 |
228 |
Вагинальное содержимое |
|
4 |
nts-012 |
Cифилис врожденный РВ++ |
98 |
1040 |
1152 |
Кровь |
|
5 |
NT-795 |
Обследование на ЗППП |
120 |
1240 |
2520 |
Кровь |
|
6 |
SF-911 |
Сифилис скрытый (состояние после лечения) |
680 |
760 |
1200 |
Эякулят |
|
7 |
SF-747 |
Обследование на ЗППП |
680 |
3280 |
4600 |
Эякулят |
|
8 |
L-ARTH |
Сифилис I серопозитивный |
1600 |
1020 |
840 |
Кровь |
|
9 |
NT-790 |
Обследование на ЗППП |
1900 |
740 |
440 |
Кровь |
|
10 |
TPLF |
Сифилис II рецидивный |
3000 |
2000 |
5600 |
Кровь |
|
11 |
ТР-1 |
Взвесь трепонем кролика |
4000* |
5000 |
9000 |
Экссудат с клетками |
* У кролика отсутствует метаболит 428, данные приведены по этилкопростанолу
Из данных таблицы следует, что предполагаемые маркеры присутствуют во всех исследованных пробах, в том числе и у практически здоровых людей. Повидимому, в обычных условиях в клетках организма человека происходит синтез кампестерола, ситостерола и стерина-428, но количество их невелико. У больных сифилисом или экспериментально зараженных животных (в случае заведомого присутствия в организме бледных трепонем) концентрация этих стеринов в биологических жидкостях существенно увеличивается. Этот уровень повышается от минимальной концентрации у доноров до средних значений у лиц из группы риска заражения ЗППП и достигает максимума у больных сифилисом и экспериментальных животных. Причем в препаратах спирохет эти вещества отсутствуют, что свидетельствует об отсутствии их синтеза вне контакта с организмом хозяина. собственно, это является известным фактом, так как бактерии не способны синтезировать стерины.
Рис. Распределение стеринов – предполагаемых маркеров бледной трепонемы в биологических жидкостях больных разных категорий и доноров.

Таким образом, установлен факт увеличения образования трех описываемых стеринов в биологических жидкостях человека и экспериментального животного в присутствии бледных трепонем. Необходимы дальнейшие исследования с целью возможного использования данного явления для обнаружения возбудителя в организме человека.
|
|
Метаболит 428 |
Ситостерол |
Кампестерол |
|
Доноры n=18 |
6 |
32 |
40 |
|
Соматические больные n=59 |
60 |
230 |
300 |
|
Обследование на ЗППП |
44 |
1110 |
228 |
|
Cифилис врожденный РВ ++ |
98 |
1040 |
1152 |
|
Обследование на ЗППП |
120 |
1240 |
2520 |
|
Сифилис скрытый |
680 |
760 |
1200 |
|
Обследование на ЗППП |
680 |
3280 |
4600 |
|
Сифилис I серопозитивный |
1600 |
1020 |
840 |
|
Обследование на ЗППП |
1900 |
740 |
440 |
|
Сифилис II рецидивный |
3000 |
2000 |
5600 |
|
Взвесь трепонем кролика |
4000 |
5000 |
9000 |
Приведенные примеры показывают, что использованный метод позволяет проводить специфический количественный анализ микробных маркеров в крови и биологических жидкостей здоровых и больных людей и надежно фиксировать разницу их концентраций. В отличие от других известных способов диагностики ГХ-МС-МФ метод не требует прекультивирования пробы, а также использования специфического биологического тестового материала: ферментов, сывороток, меток, праймеров, питательных сред, экспериментальных животных и т.п. В анализе используются химические реактивы и аппаратура, общеупотребимая при хромато-масс-спектрометрическом рутинном анализе.
На данной стадии заболевания возможно использование для диагностики хроматографа с обычным детектором (ионизации в пламени), так как концентрации диагностических стеринов достаточно велики и в их области на хроматограмме нет мешающего фона. Повидимому, можно применить и жидкостную хроматографию.
Выводы.
Благодарности.
Авторы выражают благодарность канд.мед.наук Соколову Я.А. за предоставление биологических проб и канд.хим.наук Деминой А.М. за составление реферата по методам диагностики сифилиса.
Литература.
|
|