Клинико-гормональные и эхографические параллели при синдроме гиперандрогении.
|
Синдром гиперандрогении (СГА) представляет собой патологическое состояние, обусловленное действием избыточной секреции андрогенов на органы и ткани-мишени, и является актуальной проблемой в гинекологии [1, 4, 10, 13, 19]. Клинические признаки гиперандрогении часто сочетаются с нарушением менструальной и репродуктивной функций, избыточной массой тела, нейроэндокринными и вегетативными расстройствами [1, 3, 12, 16]. Гиперандрогенная форма бесплодия занимает третье место в структуре патологии фертильности у женщин [4, 9, 20]. Все это определяет медико-социальную значимость СГА, исключительную актуальность проблемы, необходимость усовершенствования методов диагностики [2, 5, 7, 12].
Диагностика конкретной клинической формы гиперандрогении сложна, что обусловлено многофункциональностью эндокринной системы, полиморфизмом изучаемой патологии, преобладанием смешанных форм. Между тем выделение формы гиперандрогении безусловно важно для назначения адекватной, патогенетически обусловленной терапии [1, 3, 6, 11, 19]. В связи с тем, что СГА нередко сопровождается поликистозными изменениями в яичниках, особую актуальность в диагностике данной патологии приобретает эхография [5, 8, 15]. Неинвазивность, доступность, быстрота выполнения и высокая информативность делают эхографию серьезным конкурентом морфологического исследования, которое долгое время считалось определяющим в диагностике изучаемой патологии [9, 10, 12, 17, 18]. Однако возможности эхографии при обследовании больных с гиперандрогенией недостаточно изучены. В доступной литературе не рассмотрены вопросы дифференциальной диагностики различных форм гиперандрогении по эхографическому признаку. Вышеизложенное подтверждает актуальность проблемы, убеждает в необходимости совершенствования методов обследования больных с гиперандрогенией, поиска оптимальных диагностических критериев, позволяющих точно и в короткие сроки выделить форму гиперандрогении. Целью настоящего исследования явилось повышение точности диагностики и эффективности лечения больных с гиперандрогенией на основе разработки новых эхографических критериев. Материал и методы Обследованы 159 больных в возрасте от 18 до 28 лет с функциональными формами гиперандрогении, в том числе 51 пациентка с овариальной гиперандрогенией, 56 - с центральной формой гиперандрогении в сочетании с нейроэндокринным синдромом, 52 - с надпочечниковой гиперандрогенией. Из наблюдения исключены органические формы СГА (андрогенпродуцирующие опухоли яичников и надпочечников, опухоли гипофиза). Контрольную группу составили 80 здоровых фертильных женщин с регулярным менструальным циклом и отсутствием признаков гиперандрогении. Больным проводились общеклиническое, гормональное, эхографическое и морфологическое обследования. Общеклиническое обследование включало сбор анамнеза, общий и гинекологический осмотр, консультацию эндокринолога, окулиста, невропатолога. Индекс массы тела (ИМТ) оценивался по G. Brey (1978), у пациенток с ожирением рассчитывался индекс объем талии (ОТ) / объем бедер (ОБ), степень гирсутизма определялась методом D. Ferriman, J. Gallwey (1961). Гормональный скрининг состоял в определении в крови уровня ФСГ, ЛГ, пролактина, тестостерона, ДЭА-сульфата, 17-ОН-прогестерона. Для оценки состояния гипоталамо-гипофизарной системы проводились электроэнцефалография, реоэнцефалография, рентгенография черепа и турецкого седла. Для исключения органического варианта центральной и надпочечниковой форм гиперандрогении применялась компьютерная томография гипофиза и надпочечников. Эхографическое исследование яичников проводилось на ультразвуковом сканере "Esaotе AU-3" с набором датчиков трансабдоминального конвексного частотой 5 Мгц, трансвагинального частотой 7,5 МГц и выполнялось в раннюю фолликулярную фазу менструального цикла или на фоне аменореи. Материал для морфологического исследования яичниковой ткани получали с помощью лапароскопического доступа. Статистическая обработка результатов исследования осуществлялась методами вариационной статистики с использованием критерия Стьюдента. Результаты и обсуждение Клиническими симптомами СГА были нарушение репродуктивной и менструальной функций, избыточное оволосение, головная боль, ожирение.
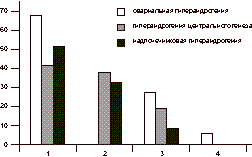
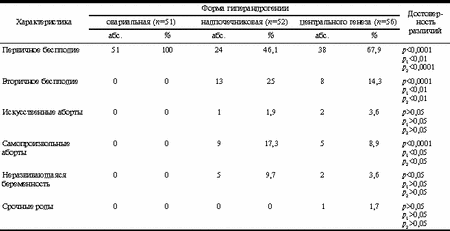
Характеристика менструальной функции у больных с гиперандрогенией. 1 - олигоменорея с менархе; 2 - олигоменорея после периода регулярных менструаций; 3 - вторичная аменорея; 4 - ациклические кровотечения. Анализ репродуктивной функции (табл. 1) показал, что единственным нарушением фертильности у больных с овариальной гиперандрогенией являлось первичное бесплодие. Вторичное бесплодие и невынашивание беременности чаще всего встречались при надпочечниковой гиперандрогении. При гиперандрогении центрального генеза наблюдались все виды нарушения репродуктивной функции. Нарушение овариально-менструального цикла присутствовало при всех формах, однако характер нарушения оказался различен (см. рисунок). Средний возраст менархе у больных с овариальной гиперандрогенией составил 13,2±1 год, у больных с центральной формой гиперандрогении - 12,5±1 год, у больных с надпочечниковой гиперандрогенией - 14±1 год. Таблица 1. Характеристика репродуктивной функции больных с СГА
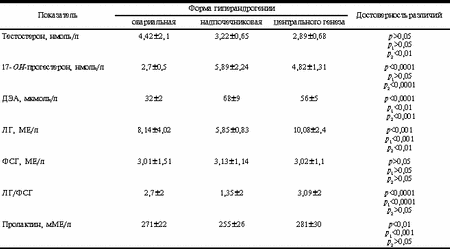
Примечание. Здесь и в табл. 2: р - различия между овариальной и надпочечниковой формой гиперандрогении; р1 - различия между надпочечниковой и центральной формой гиперандрогении; р2 - различия между овариальной и центральной формой гиперандрогении. Особенностью больных с овариальной гиперандрогенией была олигоменорея с менархе (р<0,0001). При гиперандрогении надпочечникового и центрального генеза наблюдалось нарушение менструального цикла как с менархе, так и после периода регулярных менструаций. Вторичная аменорея при надпочечниковой гиперандрогении встречалась достоверно реже (р<0,001), чем при овариальной гиперандрогении. Различий по частоте вторичной аменореи у больных с гиперандрогенией овариального и центрального генеза не обнаружено (р>0,05). Ациклические кровотечения наблюдались только у больных овариальной гиперандрогенией (5,9%). Проявления гиперандрогении в зависимости от формы СГА были различны. У больных с овариальной гиперандрогенией наблюдался невыраженный гирсутизм, начавшийся с менархе. Признаки гиперандрогенной дермопатии обнаружены у 16 (31%) женщин. У больных с надпочечниковой гиперандрогенией гирсутизм имел выраженный характер, в 38 (73%) случаях он появился до менархе. Гиперандрогенная дермопатия выявлена у 42 (80,8%) пациенток. У 5 (9,6%) больных с надпочечниковой гиперандрогенией наблюдались симптомы вирилизации. При СГА центрального генеза отмечался невыраженный гирсутизм без проявлений дермопатии и вирилизации. Гирсутное число составило у больных с надпочечниковой гиперандрогенией 16±1, у больных с овариальной гиперандрогенией 14±1, у больных с центральной формой СГА - 13±1. Избыточная масса тела наблюдалась у 38% больных, на что указывал ИМТ, равный 28±1; у 12% из них определялся висцеральный тип ожирения с ОТ/ОБ, равным 0,91±0,5. Изменения кровенаполнения головного мозга по данным реоэнцефалографии и электропроводности по данным электроэнцефалографии обнаружены у 46% больных с центральной формой гиперандрогении. Различия гормонального статуса больных с СГА в зависимости от его формы представлены в табл. 2. Согласно полученным данным, у больных с яичниковой гиперандрогенией отмечалось повышение уровня тестостерона при нормальных показателях надпочечниковых андрогенов - ДЭА и 17-ОН-прогестерона, повышение уровня ЛГ и нарушенное отношение ЛГ/ФСГ - более 2,5; в некоторых случаях (19%) наблюдалось повышение содержания пролактина в плазме крови. При надпочечниковой гиперандрогении обнаружено повышение уровня всех андрогенов - тестостерона, ДЭА, 17-ОН-прогестерона при нормальных показателях ЛГ и ФСГ и отношении ЛГ/ФСГ менее 2,5. У больных с гиперандрогенией центрального генеза выявлено повышение уровня тестостерона, ДЭА, 17-ОН-прогестерона, ЛГ, отношение ЛГ/ФСГ более 2,5, повышение концентрации пролактина в плазме крови (30,4%). Снижение уровня ФСГ обнаружено у 76,5% пациенток с яичниковой гиперандрогенией и у 80,3% больных с гиперандрогенией центрального генеза. Таблица 2. Показатели гормонов крови при различных формах гиперандрогении
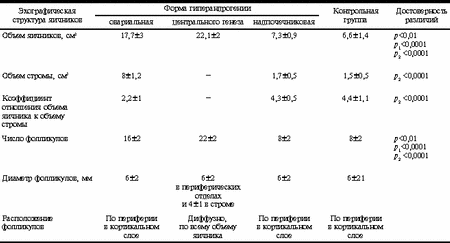
Таблица 3. Эхографическая структура яичников при различных формах гиперандрогении
Примечание. р - достоверность различий между овариальной и центральной формой гиперандрогении; р1 - между центральной и надпочечниковой формой гиперандрогении; р2 - между овариальной и надпочечниковой формой гиперандрогении. Эхографическое исследование яичников показало, что структура их различалась в зависимости от формы гиперандрогении (табл. 3). Поликистозные яичники наблюдались у больных с овариальной и центральной формами гиперандрогении, что создавало трудности в их диагностике. Однако структура поликистозных яичников при данных формах гиперандрогении оказалась различной. Объем яичников и количество фолликулов у больных с центральной формой СГА были достоверно больше, чем у пациенток с овариальной гиперандрогенией. Это обстоятельство позволило нам предположить, что у больных с центральной формой гиперандрогении возрастание объема яичников происходит в основном за счет увеличения числа фолликулов. Следовательно, вероятным источником гиперандрогении у данного контингента больных в большей степени является theca interna фолликулов, чем клетки стромы. По нашему мнению, в дифференциальной диагностике у больных с гиперандрогенией и поликистозными яичниками более перспективно изучение локализации фолликулов, определяющей тип поликистозных яичников. Согласно полученным данным, у 94% больных с овариальной гиперандрогенией наблюдался периферический тип поликистозных яичников, при котором множественные фолликулы располагались в периферическом слое яичника, а центральную часть занимала гиперплазированная строма. У 80% больных строма яичников отличалась повышенной эхогенностью за счет наличия в ней мелких гиперэхогенных включений. Для эхографической диагностики гиперплазии овариальной стромы предложено вычислять коэффициент отношения объема яичника к объему стромы. Получены численные значения коэффициента в норме 4,4±1,1 и при овариальной гиперандрогении 2,2±1,0 (р<0,0001). Таким образом, значения коэффициента 3,3 и более соответствуют норме, а значения коэффициента 3,2 и менее указывают на гиперплазию овариальной стромы. Так как гиперплазия стромы яичников является специфическим признаком овариальной гиперандрогении, можно предположить, что увеличение яичников при данной форме СГА происходит, главным образом, за счет стромальной гиперплазии, и основным источником андрогенов, вероятно, являются клетки стромы и в меньшей степени theca interna фолликулов. Диффузный тип поликистозных яичников обнаружен у всех больных с центральной формой гиперандрогении, при котором фолликулы распределялись по всему объему яичника как в его периферических отделах, так и в центральной строме. Определение истинного объема стромы и коэффициента отношения объема яичника к объему стромы при данном типе поликистозных яичников не представляется возможным. У больных с надпочечниковой гиперандрогенией структура яичников по основным эхографическим показателям не отличалась от таковой у здоровых женщин контрольной группы. Корреляционный анализ выявил у больных с овариальной гиперандрогенией прямую умеренную линейную зависимость между объемом яичников и уровнем тестостерона (r =+0,7; p<0,05), обратную выраженную линейную зависимость между коэффициентом отношения объема яичника к объему стромы и уровнем тестостерона (r =-0,92; p<0,05), обратную выраженную линейную зависимость между коэффициентом отношения объема яичника к объему стромы и показателем ЛГ/ФСГ (r =-0,82; p<0,05), прямую умеренную линейную зависимость между объемом яичников и отношением ЛГ/ФСГ (r =+0,62; p<0,05). У больных с центральной формой гиперандрогении обнаружена прямая умеренная линейная зависимость между объемом яичников и уровнем тестостерона (r =+0,69; p<0,05), выраженная прямая линейная зависимость между объемом яичников и отношением ЛГ/ФСГ (r =+0,82; p<0,05). В лечении обследованных больных использовались известные консервативные и хирургические методы. Медикаментозная терапия способствовала нормализации менструального цикла у 82,3% больных с надпочечниковой гиперандрогенией и у 88,5% больных с центральной формой, а также восстановлению фертильности соответственно у 53,6 и 52% пациенток. Согласно нашим исследованиям, оперативное лечение нецелесообразно при данных формах гиперандрогении. Анализ результатов лечения больных с овариальной гиперандрогенией показал, что консервативное лечение дало кратковременный незначительный результат в нормализации менструальной функции (у 21,6% пациенток) и оказалось неэффективным для восстановления фертильности. Оперативное лечение, выполненное 96% больных с овариальной гиперандрогенией, привело к восстановлению менструального цикла у 68,6% больных и наступлению беременности у 51% пациенток, причем у 40% из них без индукции овуляции, что свидетельствует о высокой эффективности лечения. Больным проводились клиновидная резекция и электрокаутеризация яичников. По нашим данным, эффективность лечения не зависела от техники овариотомии. Выводы Дифференциальная диагностика различных форм гиперандрогении, сопровождающихся поликистозными яичниками, возможна по эхографическим признакам. У больных с овариальной гиперандрогенией наблюдается периферический тип поликистозных яичников и объем яичников увеличен в большей степени за счет гиперплазии стромы. Для центральной формы гиперандрогении характерен диффузный тип поликистозных яичников, при котором увеличение объема яичников происходит в основном за счет повышения числа фолликулов. В качестве эхографического маркера стромальной гиперплазии у больных с овариальной гиперандрогенией целесообразно использовать коэффициент отношения объема яичника к объему стромы. Корреляция гормональных и эхографических показателей и предложенные эхографические критерии позволяют отказаться от обязательного использования гормонального метода обследования у больных с гиперандрогенией. С целью восстановления репродуктивной функции больным с овариальной гиперандрогенией целесообразно назначать оперативное лечение при следующих эхографических показателях: периферическом типе поликистозных яичников и коэффициенте отношения объема яичника к объему стромы, равным 3,2 и менее. При отсутствии данных эхографических признаков рекомендуется консервативное лечение. Н.А. Жаркин, С.А. Кузьмина Волгоградская медицинская академия, Саратовский центр планирования семьи и репродукции Литература 1. Алиева Э.А., Пшеничникова Т.Я., Гаспаров А.С., Данченко О.В. Диагностическая и оперативная лапароскопия при синдроме поликистозных яичников. Акуш и гин 1992; 2: 61-64. 2. Бронштейн М.Э. Морфологические изменения в яичниках при синдроме гиперандрогении овариального генеза. Материалы 1-го Московского съезда эндокринологов. М 1997; 186-201. 3. Вихляева Е.М. Болезнь поликистозных яичников. Азиатский вестник 1999; 5: 1-2: 60-73. 4. Гаспаров А.С., Кулаков В.И., Богданова Е.Д. Особенности клинического течения и эффективность лечения болезни поликистозных яичников в подростковом и зрелом репродуктивном возрастах. Пробл репрод 1995; 4: 18-21. 5. Демидов В.Н., Алиева Э.А., Струков А.В. Возможности эхографии в диагностике синдрома поликистозных яичников. Акуш и гин 1991; 1: 40-42. 6. Дзенис И.Г., Бахарев В.А., Фанченко Н.Д., Дуринян Э.Р., Назаренко Т.Д., Сотникова Е.И. Стероидогенез в надпочечниках при синдроме поликистозных яичников. Пробл репрод 1997; 3: 11-15. 7. Жаркин Н.А. Влияние рефлексотерапии на уровень пролактина в плазме крови при различной степени гипогалактии. Тезисы докладов Всесоюзной конференции по рефлексотерапии 6-8 июля 1987. Волгоград 1987; 338-340. 8. Клиническое руководство по ультразвуковой диагностике. Под ред. В.В. Митькова, М.В. Медведева. М 1997; 3: 132-175. 9. Кулаков В.И., Овсянникова Т.В. Значение лапароскопии в клинике бесплодия: структура и частота патологии; эффективность лечения. Пробл репрод 1996; 2: 35-37. 10. Манухин И.Б., Геворкян М.А. Синдром поликистозных яичников (клиническая лекция). Пробл репрод 1999; 6: 16-22. 11. Овсянникова Т.В., Сперанская Н.В., Глазкова О.И. Андрогены в физиологии и патофизиологии женского организма. Гинекология 2000; 2: 2: 42-44. 12. Пищулин А.А., Мальцева М.Ф., Яровая И.С., Бронштейн М.Э., Добрачева А.Д. Овариальная гиперандрогения, диагностика, лечение. Современные концепции эндокринологии. М 1999; 8-12. 13. Раисова А.Т. Актуальные проблемы гиперандрогении. Клиницист 1995; 3: 54-59. 14. Сметник В.П., Тумилович Л.Г. Неоперативная гинекология. Ст-Петербург 1995; 139-146. 15. Стрижаков А.Н., Давыдов А.И. Клиническая трансвагинальная эхография. М 1997; 121-144. 16. Barbieri R.I. Hyperandrogenic disorders. Clin Obstet Gynec 1990; 33/3: 640-654. 17. Botsis D., Kassanos D., Pyrgiotis E., Zourlas P.A. Sonographic incidente of polycystic ovaries in a gynecological population. Ultrasound-Obstet-Gynec 1995; Sept, 6(3): 182-185. 18. Farhi J., Soule S., Jacobs H.S. Effect of laparoscopic ovarian electrocautery on ovarian response and outcome of treatment with gonadotropins in clomiphene citrate-resistant patients with polycystic ovary syndrome. Fertil Steril 1995; 64: 930-935. 19. Franks S. Polycystic Ovary Syndrome. J Med 1995; 333/13: 853-861. 20. Lobo R.A. A disorder without indentity: PCO. Fertil Steril 1995; 65(6): 1158-1159. |