Диагностика редкого заболевания крови (гемофилии В (Болезни Кристмана)) у мальчика 1 года с гематомой ягодицы
Стоногин С.В., Тепаев Р.Ф., Лаврентьева И.Н., Денбург А.Д., Ручкина Е.В., Грушина Н.В.
Мальчик 1 года 10 месяцев поступил с жалобами на наличие инфильтрата в области правой ягодицы. За неделю до поступления мальчик садился на игрушки дома и после этого стал показывать своей тёте рукой на правую ягодицу, где появилось объёмное образование. Какой-то значительной травмы, удара не было. При поступлении ему выполнена пункция ягодицы, так как по данным УЗИ была картина абсцесса ягодицы - при осмотре мягких тканей правой ягодичной области в нижней-внутренней части ягодицы, участок инфильтрации без четких контуров с жидкостным включением в нем 24*9 мм на глубине 8-9 мм от поверхности кожи с небольшим количеством взвеси в нем. В зоне инфильтрации полоски жидкости шириной по 1-1.5 мм. Кровоток в зоне инфильтрации усилен. По данным эхографии абсцесс правой ягодичной области.
При пункции данного образования гноя не получено. Получена кровь. От разреза, дренирования решено воздержаться.
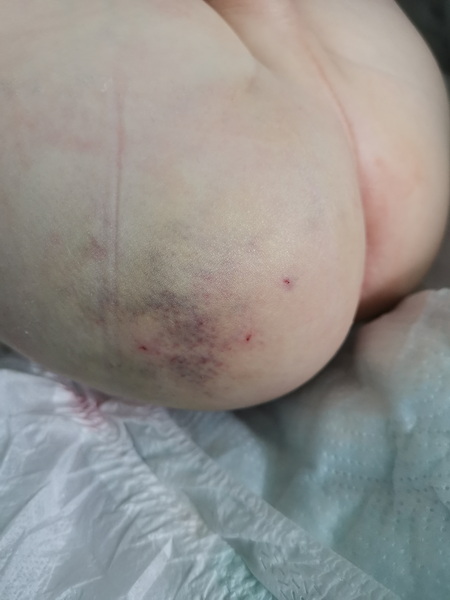
Рис 1 – вид инфильтрата ягодицы
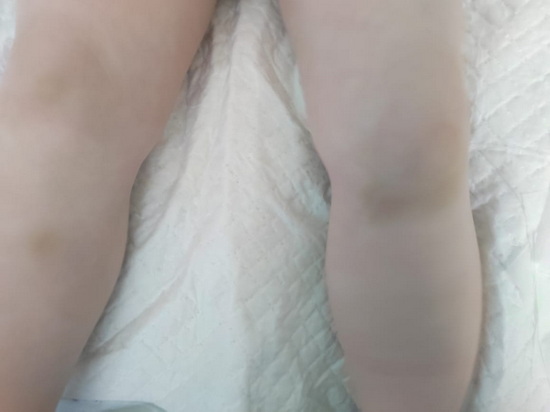
Рис 2 – в области коленных суставов экхимозы после падений на область суставов
Повторное УЗИ ягодицы - в нижнем медиальном квадранте правой ягодичной области, на глубине 12-16 мм, на ррасстоянии 6 мм ануса определяется жидкостное образование, вытянутой в поперечном сечении формой, до 55 мм, толщиной до 10 мм, разделенное на полости эхогенными утолщенными перегородками (возможно, - срезы в разных плоскостях). Создается впечатление о слоистых стенках образования. Окружающие ткани утолщены, повышенной эхогенности. В режиме цветового картирования лоцируются сосуды по периферии и перегородочных структурах. Эхопризнаки распространенного жидкостного образования правой ягодичной области.
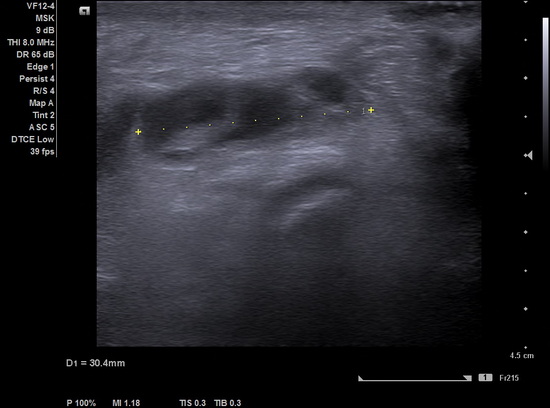
Рис 3 – УЗИ мягких тканей ягодицы
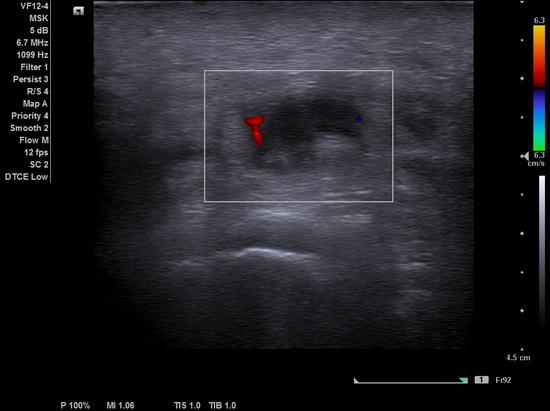
Рис 4 – УЗИ мягких тканей ягодицы
Повторное УЗИ ягодицы - в проекции правой ягодицы определяется утолщение мягких тканей до 16 мм, а также на глубине 12 мм образование неправильной формы общими размерами 43х12 мм с неровными нечеткими контурами, анэхогенное по структуре с гиперэхогенными перемычками, в режиме ЦДК кровоток не лоцируется, достоверной связи с анусом не прослеживается. Эхопризнаки отека мягких тканей, жидкостного образования правой ягодицы (гематома?).
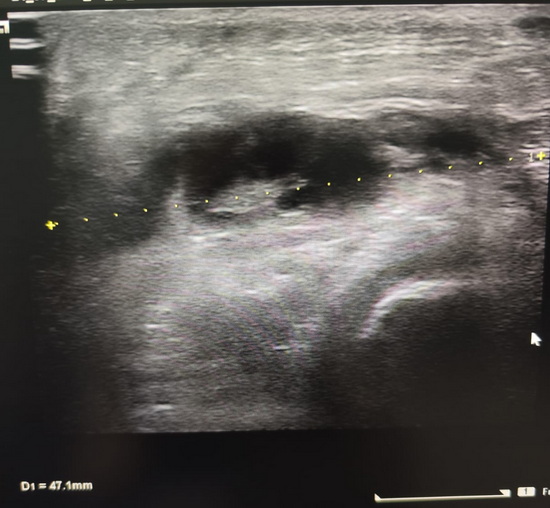
Рис 5 – повторное УЗИ мягких тканей ягодицы
Ссылка на видео узи мягких тканей ягодицы с определением кровотока - https://youtube.com/shorts/lQ-ArRomte0?feature=share
В общем анализе крови патологии нет. Выполнена коагулограмма - АЧТВ 128с, протромбин 68%. Выполнена также тромбоэластограмма. Лабораторный образец, поступивший в лабораторию на исследование гемостаза, был использован для наработки опыта сотрудников врачей-лаборантов и трансфузиолога использования прибора тромбоэластометра ROTEM. В процессе получения результата исследования, учитывая исходный изолированный резко увеличенный уровень АЧТВ, выявлены признаки коагулопатии, было заподозрено наличие гемофилии. Для дальнейшего обследования и лечения переводится в отделение гаматологии Морозовской ДГКБ, где был установлен диагноз гемофилии В. При определении IX фактора концентрация его менее 1%. Установлена тяжелая форма гемофилии В.
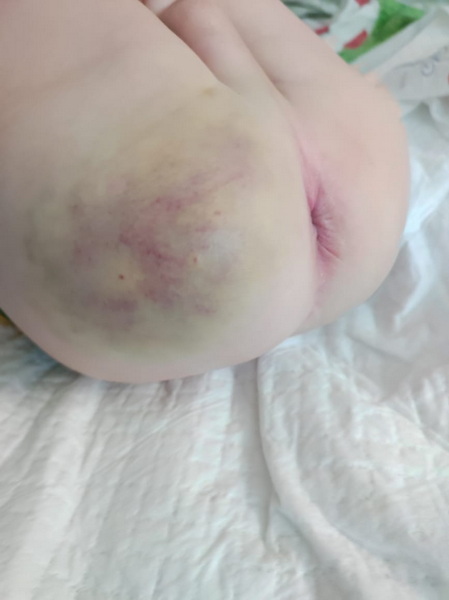
Рис 6 – постепенно гематома в области ягодицы уменьшается в размере, “цветет”.
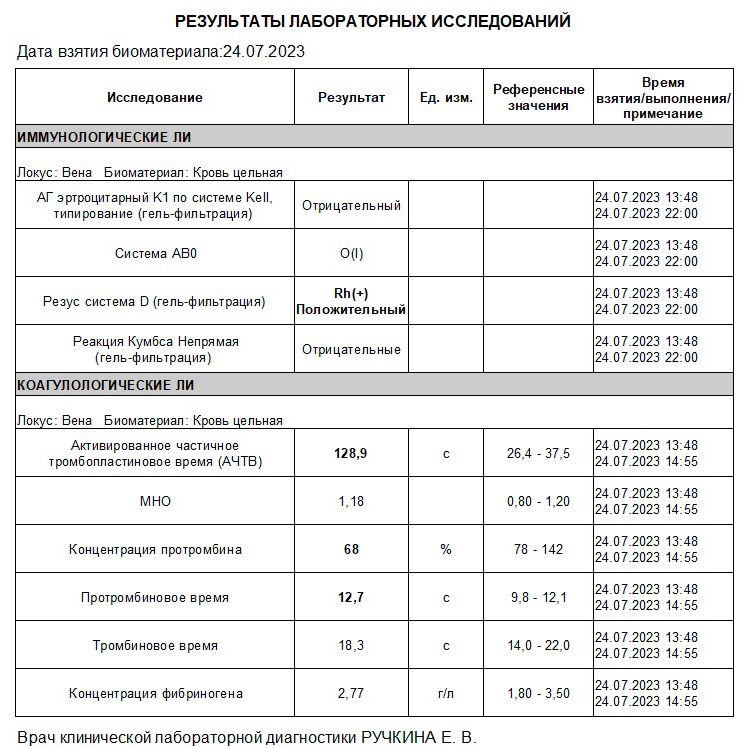
Рис 7 – коагулограмма
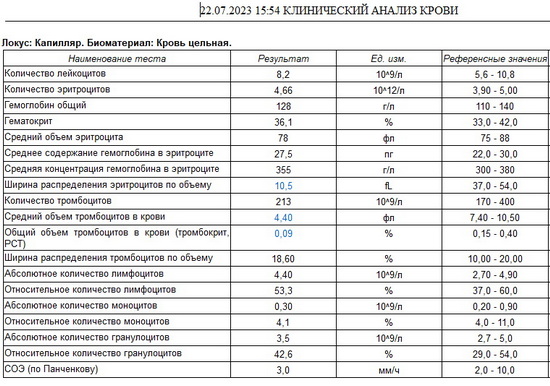
Рис 8 – общий анализ крови
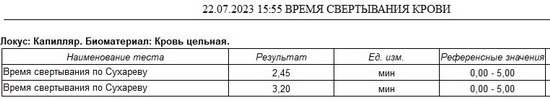
Рис 9 - гемосиндром
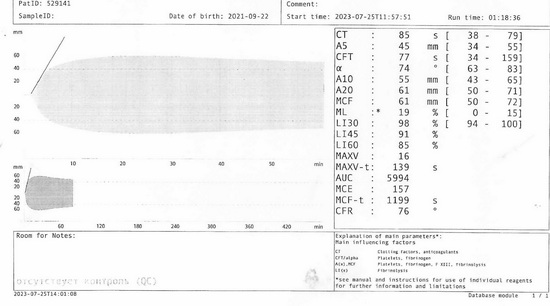
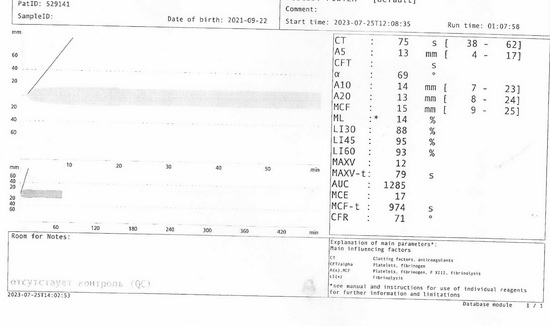
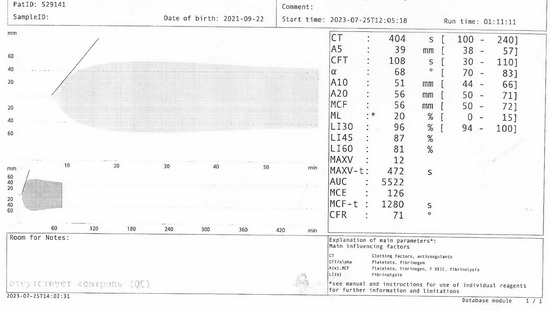
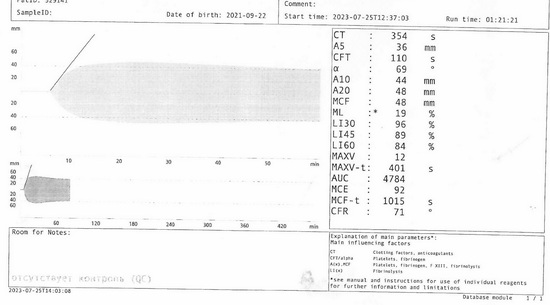
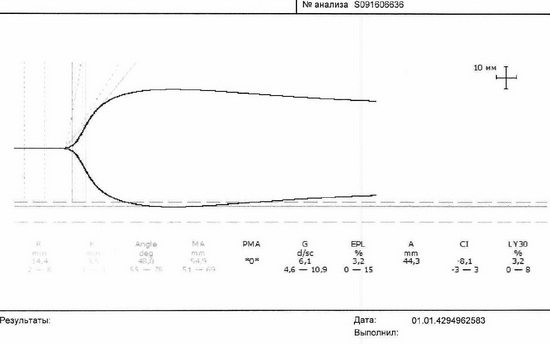
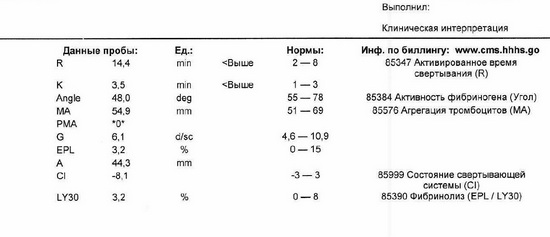
Рис 10 – тромбоэластограмма
По данным литературы, частота возникновения ингибиторов составляет 20–33% у пациентов с тяжелой формой гемофилии А (активность FVIII 1% и менее) и 0,9–7% у пациентов с легкой и среднетяжелой формой гемофилии А (активность FVIII 1–30%), 3–6,5% у пациентов с тяжелой формой гемофилии В. Ранее смертность среди больных гемофилией была в 2 раза выше, чем аналогичный показатель в общей популяции людей. Если в начале ХХ в. продолжительность жизни больных тяжелой формой гемофилии не превышала 11 лет, то к его концу колебалась уже между 58–63 годами. В США еще недавно продолжительность жизни больных гемофилией была на 10 лет меньше, чем в популяции в целом. В настоящее время продолжительность жизни больных гемофилией в США всего на 1 год меньше, чем в общей популяции. У больных гемофилией стали наблюдать проблемы и заболевания, до проявления которых они ранее просто не доживали. К таким заболеваниям относятся, например, сахарный диабет II типа, атеросклероз, гипертоническая болезнь, ишемическая болезнь, инфаркт миокарда, инсульты. Возникла необходимость терапевтического и, что важно, хирургического (например, стентирование) лечения сопутствующих приобретенных заболеваний у больных гемофилией.
В России о более высокой заболеваемости гемофилией детей из северных регионов впервые сообщила З.Д. Федорова в 1986 г. Заболеваемость гемофилией А и В в Ленинграде составляла 2,4 случая на 10 000 лиц мужского пола (т.е. 1 случай на 4166 мальчиков), что в целом соответствовало мировой статистике, но было несколько выше заболеваемости в других регионах бывшего СССР. К сожалению, в литературе не приведены данные или рабочая гипотеза о причинах более высокой заболеваемости гемофилией детей северных регионов. По сообщению О.П. Плющ, в 1969 г. в Москве регистрировался 1 больной гемофилией А и В на 42 000 жителей, что составляло 2,3 случая на 100 000 населения. Соотношение больных гемофилией А и гемофилией В составило 5:1, что соответствовало литературным данным. Данные о распространенности гемофилии в Алтайском крае приводит в своей книге З.С. Баркаган. За период наблюдения гемофилия А была выявлена у 202 (90,9%) больных, гемофилия В — у 20 (9,1%) больных, соотношение гемофилии А и гемофилии В оказалось несколько нетипичным — 10:1. Показатель заболеваемости гемофилией А составлял 1,44, гемофилией В — 0,14 на 10 000 лиц мужского пола. Представляют интерес данные, полученные в результате ретроспективного эпидемиологического исследования, проведенного в Москве на базе Гематологического центра (руководитель В.В. Вдовин) при ИДГКБ. За 25 лет (1971–1995 гг.) у жителей Москвы зарегистрировано 263 впервые выявленных случая гемофилии А и В. Ежегодно в среднем диагностировалось 8 случаев гемофилии А и 2 случая гемофилии В. Среднегодовой показатель заболеваемости мальчиков Москвы гемофилией А за анализируемый период составил 1,59±0,12, а гемофилией В — 0,39±0,06 на 10 000 живорожденных мальчиков. За 25 лет зарегистрирован только 1 случай смерти больного гемофилией от геморрагического осложнения (кровоизлияния в мозг) в результате травмы. Заболевание перестало быть смертельным у детей, все наблюдаемые больные передаются из педиатрического звена во взрослую сеть. Об этом свидетельствует и постоянно возрастающий показатель распространенности гемофилии.
Гемофилия B — заболевание, обусловленное наследственным дефицитом плазменного фактора свертывания IX, которое характеризуется кровоточивостью гематомного типа. Фактор IX (фактор Кристмаса) — компонент тромбопластина плазмы. Частота ее составляет от 1:25000 до 1:30000 рожденных мальчиков. Причиной кровоточивости является нарушение первой фазы свёртывания крови — образования тромбопластина в связи с наследственным дефицитом антигемофильного фактора. Клинически, как говорилось ранее, проявляется в гематомном типе кровоточивости, для которого характерны гемартрозы, гематомы, поздние кровотечения. В результате дефицита фактора IX кровь может не свёртываться в течение нескольких часов, из-за чего может развиться анемия.
Тяжелая форма — уровень фактора до 1 %. Геморрагический синдром проявляется в раннем детском возрасте и характеризуется частыми посттравматическими и спонтанными кровоизлияниями в суставы, мышцы, внутренние органы. У некоторых больных сразу после рождения отмечают кефалогематому, мелену, длительное кровотечение из пуповины. В последующем — продолжительные отсроченные кровотечения при прорезывании и смене молочных зубов.
Среднетяжелая форма: уровень фактора от 1 до 5 %. Характеризуется проявлением болезни в дошкольном возрасте (4–6 лет) и позже, с умеренно выраженным геморрагическим синдромом, кровоизлияниями в суставы, мышцы, гематурией. Подобные симптомы наблюдаются значительно реже, чем при тяжелой форме. Обострения геморрагического диатеза отмечаются от 2 до 3 раз в год.
Легкая форма: уровень фактора более 5 %. Отличается редкими и менее интенсивными кровотечениями. Клиническая симптоматика проявляется в школьном возрасте, после травм или операций.
Хирургов должно настораживать несоответствие тяжести полученных травм (сидел на пластиковых игрушках) и клинических проявлений (появление гематомы ягодичной области), наличие экхимозов в области коленных суставов после незначительных ушибов. Оперировать больных с гемофилией можно, но только под наблюдением гематологов, после специальной подготовки, под контролем факторов свертывания крови чтобы не было осложнений в виде кровотечений. Особенно велик риск кровотечений при поступлении больного по экстренным показаниям. При подозрении на наличие у ребенка коагулопатии необходимо определять коагулограмму со всеми показателями, включая АЧТВ. После коррекции уровня IX фактора свертывания с профилактической целью его уровня в крови хватает в среднем на 1 год. В последующем необходима повторная коррекция.
Гемостатическое обеспечение оперативных вмешательств у больных гемофилией требует решения трех важных вопросов: 1) при каких значениях FVIII или FIX в плазме обеспечиваются условия для надежного гемостаза при хирургических вмешательствах различного типа; 2) как долго необходимо поддерживать повышенную концентрацию FVIII или FIX в послеоперационном периоде; 3) из чего следует исходить в определении сроков окончания специальной гемостатической терапии, назначенной по поводу хирургического вмешательства. Наиболее быстро потребление FVIII или FIX в организме больного происходит во время операции и в ближайшие часы после нее, когда полупериод биологической активности (Т/2), например, FVIII достигает иногда 1,5 ч вместо исходных 6–8 ч. В процессе гемостатической терапии Т/2 удлиняется до 12–24 ч и при отсутствии кровотечения остается в пределах, близких к средней величине, до полного заживления тканей. Можно заранее рассчитать, при какой дозе FVIII или FIX концентрация в крови больного будет оставаться в заданных пределах в течение определенного отрезка времени, например, 24 ч. На основании этих данных была разработана тактика гемостатической терапии у больных гемофилией, нуждающихся в проведении хирургической операции. Проведение гемостатической терапии осложняется наличием индивидуальной фармакокинетики введенных препаратов у конкретных больных. Это положение обосновало необходимость проведения динамического контроля за содержанием FVIII или FIX в крови больного. Сопоставление клинических и биохимических данных позволило выделить в гемостатической терапии при хирургических вмешательствах три периода. Операционный период. Начинается с введения за 30 мин до операции FVIII или FIX в количестве, необходимом для повышения его концентрации в крови больного до избранной величины. Этот период характеризуется значительными колебаниями показателей свертывающей системы крови вследствие стресса и операционной кровопотери и требует наиболее интенсивной гемостатической и гемотрансфузионной терапии. Ближайший послеоперационный период. Характеризуется напряжением и нестабильностью процессов гемостаза вследствие преобладания в организме больного катаболических процессов, воспалительных изменений в области операции, усиленного потребления FVIII или FIX в процессе свертывания крови. В зависимости от характера и степени сложности хирургического вмешательства этот период может продолжаться от 1 до 5 дней после операции. Об окончании катаболической фазы свидетельствуют полное прекращение болей в послеоперационной ране, нормализация температуры тела, стойкое удлинение Т/2 FVIII до 17 ч и более. Эффективность гемостаза в этот период в значительной степени определяет течение репаративных процессов в поврежденных тканях. Период выздоровления. Начинается с момента окончания второго периода и продолжается до завершения основных репаративных процессов в поврежденных во время операции тканях. В этом периоде интенсивность гемостатической терапии постепенно снижают. Исследования показали, что тактика гемостатической терапии во время операции и в катаболической фазе послеоперационного периода может видоизменяться в зависимости от объема и характера хирургического вмешательства. Выделено четыре категории хирургических вмешательств по степени риска. Наивысшая категория риска. К операциям такого риска относят: радикальное удаление обширных псевдоопухолей таза и конечностей; эвакуацию обширных нагноившихся гематом в сочетании с тотальным иссечением грануляционного вала; эндопротезирование коленного и тазобедренного суставов и подобные им операции. Операционная кровопотеря при операциях этого типа составляет от 75 до 200% объема циркулирующей крови (ОЦК) пациента. Надежный гемостаз может быть получен при повышении FVIII во время операции и последующие 5 дней до 70–100%. Поддерживающие дозы факторов вводят в середине, конце операции и в последующем через каждые 12 ч в течение катаболической фазы и через 24 ч в анаболической фазе. Общая длительность терапии 3 нед. На курс лечения требуется 600 МЕ FVIII на 1 кг массы тела больного.
Высокая категория риска. К операциям такого вида относят реконструктивные операции на коленном и тазобедренном суставах, открытую репозицию и открытый остеосинтез диафизарных переломов бедра, плеча, костей голени, удаление расслаивающих забрюшинных гематом и подобные им операции. Величина операционной кровопотери составляет 25–50% ОЦК пациента. Надежный гемостаз достигается при повышении FVIII во время операции и последующие 3 дня (катаболическая фаза) до 50–70%. Поддерживающие дозы антигемофильных препаратов вводят в конце операции, через каждые 12 ч в катаболической фазе и через каждые 24 ч в анаболической фазе. Общая длительность терапии от 2 до 3 нед в зависимости от репаративных особенностей поврежденных тканей. В среднем на курс лечения требуется 500 МЕ FVIII на 1 кг массы тела больного.
Средняя категория риска. К этой группе риска относят операции на голеностопном и локтевом суставах, удаление небольших геморрагических кист и подобные им операции. Операционная кровопотеря, как правило, не превышает 15% ОЦК пациента. Надежный гемостаз может быть получен при повышении FVIII до 25–40% во время операции и последующий день. Поддерживающие дозы факторов вводят через каждые 24 ч, как в катаболической, так и в анаболической фазах послеоперационного периода. Общая длительность гемостатической терапии не превышает 7–10 дней. На курс лечения требуется 300 МЕ FVIII на 1 кг массы тела больного.
Умеренная категория риска. К этой группе риска относят небольшие по объему и малотравматичные операции типа удлинения ахиллова сухожилия и все операции, обычно выполняемые в амбулаторных условиях. Кровопотеря, как правило, не превышает 100–150 мл. Гемостаз достигается при повышении FVIII до 30–40%. Поддерживающие дозы антигемофильных препаратов вводят через каждые 24 ч в течение всего послеоперационного периода, который составляет 5–7 дней. На курс лечения требуется 170 МЕ FVIII на 1 кг массы тела больного.
При экстракции зуба FVIII или FIX назначают в виде разовой дозы, рассчитанной так, чтобы повысить активность фактора в плазме больного до 50–100% от нормы. Транексамовую кислоту применяют в качестве ингибитора фибринолиза внутривенно в дозе 10 мг на 1 кг массы тела больного перед экстракцией зуба, после чего препарат назначают в таблетках — по 2–3 таблетки по 0,5 г 3 раза в день в течение 1 нед. Дальнейшего дополнительного введения фактора FVIII или FIX не требуется, и больной переводится на обычную терапию. В случаях легкой формы гемофилии дозировка может быть сокращена в соответствии с исходной концентрацией FVIII или FIX у конкретного больного. Необходимо подчеркнуть важность длительной послеоперационной заместительной терапии в хирургическом лечении больных гемофилией, которая предупреждает развитие поздних гематом, особенно после тяжелых операций.
Литература
Румянцев А.Г., Румянцев С.А., Чернов В.М. Гемофилия в практике врачей различных специальностей, Москва,” Гэотар-Медиа”, 2012.
Данные об авторах:
- Стоногин Сергей Васильевич – врач-хирург хирургического отделения ГБУЗ ДГКБ имени З.А. Башляевой ДЗМ, кандидат медицинских наук. E-mail: svas70@mail.ru Адрес: 125480 Москва, улица Героев Панфиловцев, дом 28, отделение хирургии. https://orcid.org/0000-0003-3531-5849
- Тепаев Рустэм Фаридович – руководитель службы анестезиологии-реанимации ДГКБ им З.А. Башляевой ДЗМ, д.м.н., профессор кафедры педиатрии с курсом детской ревматологии 1-го МГМУ И.М. Сеченова. адрес: 125480 Москва, улица Героев Панфиловцев, дом 28, отделение реанимации, rtepaev@inbox.ru, http://orcid.org/0000-0001-6667-9472
- Лаврентьева Инна Николаевна – заведующая отделением гематологии Морозовской ДГКБ, Москва, 4-й Добрынинский переулок, дом 1/9, корпус 1 «А», 2 этаж, 9598800@morozdgkb.ru
- Денбург Александра Дмитриевна – врач-трансфузиолог ГБУЗ ДГКБ имени З.А. Башляевой ДЗМ. Адрес: 125480 Москва, улица Героев Панфиловцев, дом 28
- Ручкина Елена Владимировна – врач клинической лаборатории ГБУЗ ДГКБ имени З.А. Башляевой ДЗМ. Адрес: 125480 Москва, улица Героев Панфиловцев, дом 28, отделение хирургии.
- Грушина Наталья Валерьевна – врач отделения лучевой диагностики ГБУЗ ДГКБ имени З.А. Башляевой ДЗМ. 125480 Москва, улица Героев Панфиловцев, дом 28, отделение лучевой диагностики, e-mail: Natali5462@yandex.ru, https://orcid.org/0009-0000-7036-756X